REPORT AIFM
TOMOGRAFIA COMPUTERIZZATA: DESCRIZIONE E MISURA DEI PARAMETRI CARATTERISTICI
Traduzione, revisione e integrazione del documento :
“Measurement of the performance Characteristics of Diagnostic X-ray Systems used in Medicine”
Part III : Computed Tomography X-ray Scanners
(II edition)
Report N.32 IPEM (2003)
Curatore :
Paola Colombo Azienda Ospedaliera Niguarda Ca’ Granda , Milano
Autori:
Paola Colombo Azienda Ospedaliera Niguarda Ca’ Granda , Milano
Daniela Origgi Istituto Europeo di Oncologia, Milano
Luca Moro Fondazione Salvatore Maugeri, Istituto Scientifico di Pavia
Lorella Mascaro Spedali Civili Brescia
Sara Re Casa di Cura S. Maria, Castellanza
Sabrina Vigorito Istituto Europeo di Oncologia, Milano
Nicoletta Paruccini Azienda Ospedaliera S. Gerardo, Monza
Felicita Luraschi Istituti Ospedalieri di Cremona
Hanno collaborato
Caterina Ghetti Azienda Ospedaliera di Parma
Sabina Strocchi Ospedale di Circolo e Fondazione Macchi
e tutti i componenti del gruppo AIFM “TC Multistrato“
Si ringrazia
Giampiero Tosi
Guido Petroli
Luisa Pierotti
Per il prezioso lavoro di revisione
INDICE1 INTRODUZIONE 6
1.1 Sistemi di rivelazione 6
1.2 Metodi di ricostruzione lungo z 8
1.3 Cone Beam 12
1.4 Metodi di riduzione della dose 14
1.4.1 Modulazione lungo l’asse z 14
1.4.2 Modulazione angolare 15
2 FANTOCCI PER LA VALUTAZIONE DELLE IMMAGINI TCMS 18
2.1 Fantocci specifici per la qualità immagine 18
2.1.1 Fantocci per la valutazione di uniformità del n. TC, n. TC dell’acqua e rumore 18
2.1.2 Fantocci per la valutazione dello spessore dello strato 18
2.1.3 Fantocci per la valutazione dello Slice Senaitivity Profile (SSP) 19
2.1.4 Fantocci per la valutazione della risoluzione spaziale: 20
2.1.5 Fantocci per la valutazione della linearità dei numeri TC 21
2.1.6 Fantocci per la valutazione della relazione fra densità elettronica e n. TC 22
2.1.7 Fantocci per la valutazione del basso contrasto 22
2.1.8 Artefatti (Cone Beam) 24
2.2 Misure dosimetriche: strumentazione e fantocci 25
3 PARAMETRI DI QUALITA’ DELL’IMMAGINE 27
3.1 Rumore 27
3.1.1 Definizione e introduzione 27
3.1.2 Metodo di misura 27
3.1.3 Tecnica spirale 28
3.1.4 Tecnologia multistrato 29
3.1.5 Condizioni operative 29
3.1.6 Dispositivo di prova 30
3.2 Risoluzione spaziale 30
3.2.1 Definizione e discussione 30
3.2.2 Metodi 31
3.2.3 Tecnica spirale 32
3.2.4 Tecnica multistrato 32
3.2.5 Condizioni operative 32
3.2.6 Prova di accettazione e Controlli periodici 33
3.2.7 Dispositivo di prova 33
3.2.8 Risoluzione lungo l’asse z 34
3.3 n. TC e linearità 34
3.3.1 Definizione e discussione 34
3.3.2 Metodi di misura 34
3.3.3 Condizioni operative 35
3.3.4 Dispositivo di prova 35
3.4 Uniformità dei numeri TC 35
3.4.2 Definizione e discussione 35
3.4.2 Metodo di misura 35
3.4.3 Tecnica spirale 36
3.4.3 Condizioni operative 36
3.4.4 Commenti 36
3.4.5 Dispositivo di prova 36
3.5 Risoluzione a basso contrasto 37
3.5.1 Definizione e discussione 37
3.5.2 Metodi di misura 39
3.5.3 Condizioni operative 40
3.5.4 Dispositivo di prova 41
3.6 Artefatti 41
3.6.1 Definizione e discussione 41
3.6.1.1 Processi di interpolazione lungo l’asse z 42
3.6.1.2 Geometria del fascio radiante 44
3.6.1.3 Elaborazioni tridimensionali 45
3.6.1.4 Inclinazione del gantry 47
3.6.1.5 Diversa risposta dei singoli canali di acquisizione 47
3.6.2 Metodi di misura 47
4 CARATTERISTICHE DELLO STRATO 50
4.1 Spessore irradiato 50
4.1.1 Metodi di misura 50
4.1.2 Considerazioni per tomografi multistrato 51
4.1.3 Condizioni operative 51
4.2 Spessore dello strato 51
4.2.1 Metodi di misura: modalità assiale 51
4.2.2 Metodi di misura: modalità spirale 52
4.2.3 Metodi di misura: tomografi multistrato 54
4.3 Efficienza geometrica 54
4.3.1 Efficienza geometrica lungo l’asse z 54
4.3.2 Efficienza geometrica del sistema di rivelazione 56
5 INDICI DI DOSE 58
5.1 Indice di Dose per Tomografia Computerizzata (CTDI) 58
5.1.1 Definizioni 58
5.1.2 Metodi di misura 58
5.1.3 CTDI pesato (CTDIw) 60
5.1.4 CTDIvol (CTDIW mediato lungo asse z) 61
5.2 MSAD (Multiple scan average dose) 61
5.2.1 Definizione e discussione 61
5.2.2 Relazione tra CTDI e MSAD 62
5.3 Modalità spirale 63
5.3.1 TC multistrato 63
5.3.2 Condizioni operative 63
5.3.3 Commenti 64
5.3.4 Strumentazione utilizzata 65
5.4 Prodotto dose lunghezza (DLP) 65
5.5 Nuove definizioni – ICRU 74 66
6 DOSIMETRIA DEL PAZIENTE 67
6.1 Confronti dosimetrici 67
6.1.1 Confronto tra tomografi 67
6.1.2 Confronto tra protocolli 67
6.1.3 Confronto tra rischi 67
6.2 Dose superficiale e agli organi 67
6.3 Dose Efficace 68
7. Il parametro Q 69
8. VERIFICHE DI ACCURATEZZA MECCANICA 71
8.1. Introduzione 71
8.2 Tomografi computerizzati per impiego diagnostico 71
8.3 Tomografi computerizzati per impiego in ambito radioterapico 71
9 RICOSTRUZIONI MULTIPLANARI E 3-DIMENSIONALI 72
Appendice I – Riferimenti relativi ai fantocci, camere a ionizzazione e software 73
Fantocci per QA 73
Fantocci per Densità elettronica 73
Camere a ionizzazione tipo “pencil” 73
Fantocci per la misura del CTDI in PMMA (perspex) 73
Dati e software sulla dose 73
Indirizzi dei costruttori e dei fornitori 73
Schema dei principali fantocci per QA 74
Appendice II TC-PET 77
Introduzione 77
Registrazione di immagini TC/PET 77
Accuratezza di registrazione 79
Correzione per l’attenuazione 79
Dipendenza dall’energia delle mappe di attenuazione 79
Dose 80
Appendice III PROTOCOLLO PROVE DI ACCETTAZIONE 81
Introduzione 81
Esame a vista e prove di funzionamento 81
Alta Tensione e Filtrazione totale (opzionali) 81
Qualità dell’immagine 81
Rumore 81
Uniformità dei numeri TC 81
N. TC e linearità 81
Risoluzione spaziale 81
Risoluzione a basso contrasto 82
Risoluzione spaziale lungo Z 82
Artefatti 82
Caratteristiche dello strato 82
Spessore dello strato 82
Spessore irradiato 82
Efficienza geometrica 82
Indici di dose 82
CTDI in aria 82
CTDIw in fantoccio 82
CTDIvol in spirale 83
Accuratezza meccanica e controlli geometrici 83
BIBLIOGRAFIA 84
1 INTRODUZIONE
I tomografi computerizzati multistrato (TCMS) rappresentano un’evoluzione dei tomografi computerizzati spirale introdotti agli inizi degli anni 90. Si basano sull’acquisizione simultanea di più strati del paziente. I TCMS possono essere utilizzati sia in modalità assiale che spirale, ed è in questa seconda modalità che trovano un impiego più innovativo.
I vantaggi che i TCMS offrono rispetto ai sistemi a singolo strato sono la possibilità di eseguire la stessa acquisizione in tempi più brevi, o analogamente di effettuare scansioni di volumi maggiori nello stesso intervallo di tempo, di ridurre gli artefatti legati al movimento del paziente, di acquisire strati sottili, migliorando la risoluzione spaziale lungo l’asse z; ciò determina un netto miglioramento della qualità delle immagini ricostruite, quali le ricostruzioni volumetriche e multiplanari.
Di primaria importanza, nei TCMS, è la versatilità nella ricostruzione delle immagini, cioè la possibilità di ricostruire spessori di strato diversi da quelli acquisiti: ad esempio, facendo un’acquisizione assiale 16 × 1.5 mm (dove 16 indica il numero di canali di rivelazione e 1.5 mm le dimensioni del rivelatore), combinando i dati provenienti da più rivelatori, si possono ricostruire strati da 1.5, 3, 4.5 e 6 mm etc. Tale versatilità è ancora maggiore in modalità spirale, dove lo spessore dello strato ricostruito, la posizione e l’intervallo di ricostruzione possono essere scelti retrospettivamente in modo libero, senza ovviamente andare al di sotto della dimensione minima del canale di rivelazione utilizzato.
Il rapido diffondersi di tali sistemi rende necessario l’approfondimento dei metodi di acquisizione e delle prestazioni, sia in termini di qualità dell’immagine che in termini di dose. Scopo di questo documento è la descrizione dettagliata dei parametri fisici e dosimetrici più significativi per un sistema TC di concezione attuale (multistrato o no) da utilizzarsi durante le prove di accettazione [1] o costanza. Nella prima parte viene analizzato il sistema di acquisizione (geometria del sistema di rivelazione, numero di canali di ricezione, configurazione e filtri di ricostruzione lungo l’asse z). Nelle parti successive vengono definiti i metodi di verifica della qualità dell’immagine e della dose, che sono generalmente derivati da quelli per tomografi a singolo strato; per le acquisizioni in spirale può essere necessario modificare i metodi di misura o introdurre nuovi parametri di qualità (es.: l’analisi degli artefatti).
1.1 Sistemi di rivelazione
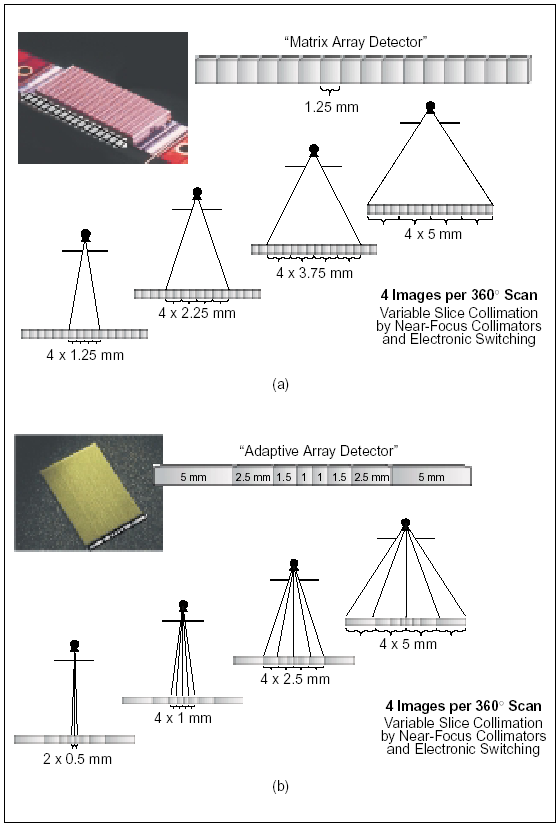
Per poter acquisire simultaneamente più strati del paziente sono necessari una matrice bidimensionale di rivelatori e un sistema di canali di rivelazione che preleva il segnale da uno o più rivelatori uniti elettronicamente (figura 1.1). Il fascio di raggi X è collimato vicino alla sorgente di radiazione nella maniera tradizionale e la definizione dell’ampiezza dello strato avviene attraverso una combinazione elettronica dei segnali; il numero massimo di strati acquisibili contemporaneamente è determinato del numero di canali di rivelazione utilizzati e dalla collimazione.
Figura 1.1: rivelatori a matrice fissa e a matrice adattativa [2]
Diverse sono state le soluzioni sviluppate dalle case produttrici di tomografi nella costruzione di matrici di rivelatori per TCMS, che possono essere classificati in tre gruppi [2]:
In tutti i casi la matrice è costituita da rivelatori allo stato solido.
Il tipo di matrice influenza la minima ampiezza dello strato che può essere ricostruito, il numero di strati di ampiezza minima, il range di spessori disponibili, la massima lunghezza che può essere campionata in una sola rotazione e l’efficienza geometrica: le matrici di tipo adattative, ad esempio, hanno il vantaggio di minimizzare gli spazi morti tra i rivelatori, in quanto gli elementi di dimensioni maggiori non contengono “setti” e non causano quindi una diminuzione dell’efficienza.
Nella figura 1.1 sono riportati esempi delle prime due classi di rivelatori per sistemi a 4 strati.
La classificazione sopra riportata risulta in realtà valida solo per sistemi con un numero di strati fino a 4 o 8; per tali sistemi i rivelatori a matrice fissa sono utilizzati nei tomografi GE, quelli a matrice adattativa nei sistemi Philips e Siemens, quelli di tipo ibrido nei sistemi Toshiba.
Attualmente tutti i tomografi a 16 strati disponibili in commercio hanno adottato una matrice di tipo “ibrido” con un numero di elementi sottili al centro (16) e altri (8-24) più spessi in periferia, mentre i sistemi a 64 strati sono a matrice fissa. In tabella 1.1 sono riportate le caratteristiche di alcuni TCMS a 16 strati.
GE Lightspeed16 | Siemens Sensation 16 | Philips Brilliance CT 16 | Toshiba Aquilion 16 | |
Gantry | ||||
Generazione | III | III | III | III |
Apertura (cm) | 70 | 70 | 70 | 72 |
FOV massimo (cm) | 50 | 50 | 50 | 50 |
Spessore dello strato nominale per scansioni assiali (mm). | 0.625, 1.25, 2.5, 3.75, 5, 7.5, 10 | 0.6, 0.75, 1, 1.5, 2, 3, 4.5, 5, 6, 9, 10 | 0.75, 1.5, 3, 6, 12 | 0.5, 1, 2, 3, 4, 6, 8 |
Sistema di rivelazione | ||||
Tipo di rivelatori | Stato solido | Stato solido | Stato solido | Stato solido |
Numero di rivelatori per fila | 888 | 672 | 672 | 896 |
Numero di elementi lungo l'asse z | 24 | 24 | 24 | 40 |
Lunghezza effettiva di ogni elemento all'isocentro (mm). | 16×0.625, 8×1.25 | 16×0.75, 8×1.5 | 16×0.75, 8×1.5 | 16×0.5, 24×1 |
Lunghezza effettiva totale dell'array di rivelatori all'isocentro (mm) | 20 | 24 | 24 | 32 |
Tabella 1.1: TCMS a 16 strati [3]
Ad oggi la tecnologia ha portato allo sviluppo di sistemi con un numero di strati maggiore di 16: un sistema a 40 e 64 strati (Philips) un sistema a 64 canali di ricezione (2x32 con macchia focale dinamica) della Siemens, un sistema a 64 strati della GE e della Toshiba.
La ricerca di tomografi con un numero maggiore di canali di rivelazione e con un’apertura del fascio sempre più ampia ha portato allo studio di sistemi TC che sfruttino le tecnologie della radiologia digitale, ed in particolare i Flat Panel Detectors (FPD); al momento i FPD forniscono ottime prestazioni nell’imaging di strutture ad alto contrasto con un’alta risoluzione spaziale, ma la risoluzione a basso contrasto, la risoluzione temporale e l’efficienza in termini di dose non raggiungono i livelli di rivelatori dedicati per TC.
1.2 Metodi di ricostruzione lungo z
Prima di analizzare i metodi di ricostruzione lungo l’asse z nei TCMS è opportuno richiamare i principi di base delle tecniche di ricostruzione dei tomografi computerizzati a spirale.
In tali sistemi si compie una scansione continua nello spazio e nel tempo; il lettino avanza con continuità, mentre il sistema tubo-rivelatori ruota.
Si definisce pitch dosimetrico o pitch× (p×) il rapporto tra l’avanzamento del lettino (t) per una rotazione di 360° e la collimazione totale dello strato x (x = N × T, dove N è il numero di strati e T lo spessore nominale dello strato):
(1.1)
Tale definizione è valida sia per tomografi a singolo strato (N = 1) che per i TCMS [4].
Per i TCMS si può avere anche un’altra definizione di pitch (pd) che non considera la collimazione totale ma l’ampiezza del singolo rivelatore d:
(1.2)
Il pitchd si ottiene quindi moltiplicando il pitchx per il numero di strati.
La definizione 1.2 è tuttavia poco usata e induce a una confusione di termini; in generale con il termine generico pitch ci si riferisce alla 1.1.
Solitamente si utilizzano valori di pitch inferiori a 2. Il valore di px è generalmente maggiore o uguale a 1 per riuscire a coprire un determinato volume nel minor tempo possibile e ridurre in questo modo la dose rispetto alla TC assiale; per i tomografi a singolo strato il pitch non deve superare il valore 2 per escludere “gap” nel campionamento lungo l’asse z.
La ricostruzione delle immagini nella TC spirale è simile a quella che si ha nei sistemi assiali: si utilizzano gli stessi algoritmi e kernel di convoluzione. Tuttavia nei sistemi spirale è richiesto un altro passaggio, la cosiddetta “interpolazione z”, il cui scopo è quello di generare un set di dati planari per una posizione arbitraria dell’immagine zR: infatti, nelle acquisizioni spirale solo una proiezione è acquisita esattamente nel piano delle immagini, le altre sono ottenute interpolando i dati spirale. Una volta ottenuto il set di proiezioni assiali, la ricostruzione planare avviene secondo le usuali procedure, solitamente basate sulla convoluzione delle proiezioni e delle tecniche di backprojection . Nella tabella 1.2 è riportato uno schema delle fasi della formazione dell’immagine nella TC convenzionale e nella TC spirale.
TC convenzionale | TC spirale | |
Scansione | n*360° scansioni in posizioni da z1 a zn | una scansione di n*360° dalla posizione z1a zn |
TC convenzionale | TC spirale | |
preprocessing | Correzioni e filtrazione | Correzioni |
TC convenzionale | TC spirale | |
Passaggio intermedio | interpolazione z |
TC convenzionale | TC spirale | |
Ricostruzione delle immagini | convoluzione e retroproiezione | convoluzione e retroproiezione |
TC convenzionale | TC spirale | |
Risultato | n immagini in posizioni da z1 a zn | Immagini in posizioni arbitraria zR tra z1 e z n |
Tabella 1.2: formazione dell’immagine nella TC convenzionale e spirale [2]
Il metodo più semplice di interpolazione z consiste nell’interpolare linearmente i dati misurati (in corrispondenza di una determinata posizione angolare) appena prima e dopo la posizione zR del lettino; tali posizioni distano d lungo l’asse z e 360° lungo la traiettoria spirale (figura 1.2). Tale algoritmo è indicato come 360°LI.
Figura 1.2: algoritmo di interpolazione 360° LI [2]
Un altro metodo di interpolazione tiene conto della ridondanza dei dati in una scansione di 360°: in ogni rotazione completa del tubo a raggi X ogni valore di una proiezione è misurato due volte da due raggi opposti. Utilizzando delle procedure di rebinning (riordinamento) dei dati, questa ridondanza fornisce la possibilità di determinare la proiezione in una posizione angolare arbitraria a partire dalle proiezioni misurate in direzioni opposte che distano 180° (algoritmo 180° LI, figura 1.3).
Figura 1.3: algoritmo di interpolazione 180° LI [2]
Passando a sistemi multistrato le spirali di dati disponibili sono molte e pertanto è possibile interpolare dati da spirali vicine piuttosto che dalla stessa spirale di dati.
Il principio dell’interpolazione z è indipendente dal numero M di strati acquisiti contemporaneamente, come si può osservare confrontando la figura 1.3 con la figura 1.4. In entrambi i casi, per ogni posizione angolare si selezionano per l’interpolazione z i valori misurati che sono più prossimi alla posizione zR desiderata. In questo caso si parla di algoritmo 180°MLI, perché si considerano M strati per effettuare un’interpolazione z con algoritmo 180°LI.
Figura 1.4: algoritmo di interpolazione 180° MLI [2]
Benché questa possa essere considerata l’interpolazione “base”, in realtà nei TCMS, disponendo di molti dati, si utilizzano metodi di z-filtering più elaborati: i dati provenienti dalle spirali vicine alla sezione da ricostruire vengono opportunamente “pesati” e utilizzati per ricostruire al meglio lo strato desiderato. Con questo algoritmo di ricostruzione il profilo dello strato, il rumore e gli artefatti nell’immagine sono quindi determinati non solo dai parametri di scansione (pitch, collimazione del fascio, mA, tempo) ma anche dai parametri utilizzati durante lo z-filtering [5].
Figura 1.5: z-filtering [2]
1.3 Cone Beam
Il passaggio dalla scansione di uno o pochi strati all'acquisizione volumetrica (TCMS > 4 strati) implica il passaggio da una geometria tipo fan beam ad una di tipo cone beam; in realtà non esiste in letteratura una definizione esatta che indichi quando un fascio passi da fan a cone. Tuttavia si assume che se l’angolo sotteso dai rivelatori esterni è minore di 1° allora i raggi opposti per un rivelatore esterno avranno un offset inferiore allo spessore dello strato, quindi il fascio è di tipo fan e la geometria può essere considerata planare.
Al contrario, se l’angolo sotteso dai rivelatori esterni è maggiore di 1° allora i raggi opposti per un rivelatore esterno, avranno un offset superiore allo spessore dello strato, quindi il fascio è di tipo cone e devono essere considerati degli appropriati algoritmi di ricostruzione di tipo Cone Beam (CB).
La prima condizione è verificata per sistemi con un numero di strati inferiore o pari a 4, per i quali può essere trascurata la divergenza del fascio [6].
L’effetto CB è illustrato in figura 1.6: man mano che il sistema tubo-rivelatori ruota attorno al paziente, dettagli dell’oggetto appartenenti a uno stesso piano vengono “visti” da due diversi rivelatori. Questo porta alla formazione di artefatti, che sono più evidenti per le file di rivelatori più esterne che per quelle interne: i dettagli presenti nell’oggetto che si trovano in posizione lontana dall’asse sono proiettati su diverse file di rivelatori per differenti angolazioni del tubo; gli artefatti derivanti da questa errata registrazione dei dati saranno tanto più evidenti quanto maggiore è l’angolo del cono e quanto più sottile è lo strato (e maggiore è il numero di strati acquisiti simultaneamente).
Per risolvere tali problemi, le case produttrici di TCMS impiegano, per tomografi a 8 e 16 strati, algoritmi di ricostruzione CB invece dell’interpolazione lungo l’asse z. Tali algoritmi di ricostruzione possono essere divisi in due classi:
Gli algoritmi esatti tendono a convertire i dati proiettivi misurati (integrali di linea) nello spazio dei “Radon-data”. Le formule di conversione non contengono approssimazioni, da cui il nome di algoritmi esatti. Lo svantaggio di questi algoritmi consiste soprattutto nei tempi di ricostruzione delle immagini che male si adattano alla pratica clinica; questi algoritmi non sono implementati sui tomografi attualmente in commercio.
Figura 1.6: l’effetto cone beam [15]
Gli algoritmi approssimati introducono invece delle approssimazioni più o meno severe per invertire i dati cone beam. Tali algoritmi sono divisi a loro volta in due classi, quelli di Slice Rebinning e quelli basati sulla teoria di Feldkamp.
Tra gli algoritmi di Slice Rebinning occorre menzionare l’ASSR (Advanced Single Slice Rebinning), che utilizza un intervallo parziale della scansione (240°) per la ricostruzione delle immagini. I piani delle immagini non sono più perpendicolari all’asse del paziente ma sono inclinati per meglio adattarsi alla traiettoria a spirale della macchia focale. Le immagini assiali sono ottenute facendo un’interpolazione tra i piani dell’immagine inclinati (figura 1.7).
I metodi di ricostruzione basati sulla teoria di Feldkamp trattano ogni voxel individualmente, piuttosto che come parte di uno strato assiale, e fanno uso della divergenza del fascio lungo l’asse z. Per un determinato angolo di proiezione, un voxel può utilizzare un raggio proveniente da una rotazione, mentre un altro voxel nello stesso piano assiale utilizza un raggio proveniente da un’altra rotazione. In questo modo si produce un array tridimensionale di voxel a partire dal quale si possono ricostruire immagini in ogni piano.
Nella tabella 1.3 sono riportati gli algoritmi di Cone Beam utilizzati dalle diverse Ditte produttrici di tomografi multistrato (8, 16 e 64 strati).
Ditta | Algoritmo CB |
GE | Cross Beam e Hyperplane reconstruction (Slice rebinning) |
Siemens | AMPR (Slice rebinning, basato su ASSR) |
Toshiba | Coneview (Feldkamp) |
Philips | COBRA (Feldkamp) |
Tabella 1.3: algoritmi CB
Si tenga conto tuttavia della continua evoluzione e ricerca da parte delle ditte costruttrici di questi metodi e algoritmi, al fine di ridurre in modo sempre più efficace gli artefatti con il minor tempo di ricostruzione.
Figura 1.7: Algoritmi di Slice rebinning: ASSR [15]
1.4 Metodi di riduzione della dose
Modulazione della corrente nel tubo
Un parametro chiave che influisce sulla dose al paziente è il prodotto tra la corrente nel tubo e il tempo di esposizione (mAs). A parità di tutti gli altri parametri di scansione, una riduzione della corrente al tubo comporta una riduzione della dose al paziente e un aumento del rumore nelle immagini. E’ possibile impostare manualmente la corrente nel tubo sulla base del peso e delle dimensioni del paziente per cercare di ottenere un compromesso tra rumore e dose al paziente. Questo approccio però non consente di avere una qualità dell’immagine costante lungo tutta la sezione esaminata. Le tecniche di modulazione automatica della corrente nel tubo (Automatic Tube Current Modulation - ATCM) permettono di mantenere una qualità dell’immagine costante per una determinata selezione di parametri di esposizione impostati in quanto rispondono in maniera rapida alle variazioni di attenuazione del fascio. Le tecniche di modulazione di dose possono essere paragonate a quelle di controllo automatico dell’esposizione (AEC) in radiologia convenzionale [8, 9, 10].
Il principio su cui si basa la modulazione della corrente è che il rumore del pixel nella scansione TC è legato al rumore quantico delle proiezioni. Modulando la corrente nel tubo in relazione alle variazione dell’anatomia del paziente il rumore quantico della proiezioni può essere mantenuto a un livello scelto dall’utilizzatore.
Attualmente sono disponibili due tecniche per di ATCM:
1.4.1 Modulazione lungo l’asse z
La corrente nel tubo viene modulata rotazione per rotazione tenendo conto della variazioni nell’attenuazione lungo l’asse z del paziente. In questo modo il livello medio di rumore in uno strato si mantiene approssimativamente costante per diverse posizioni lungo l’asse z
Figura 1.8: modulazione lungo l’asse z [37]
1.4.2 Modulazione angolare
La modulazione avviene durante ogni singola rotazione, in modo tale da compensare grosse deviazioni dalla simmetria circolare del paziente: ad esempio in corrispondenza delle spalle i fasci provenienti anteriormente sono molto meno attenuati rispetto a quelli laterali e quindi l’intensità del fascio anteriore può essere ridotta senza compromettere in modo importante la qualità immagine.
Sono riportate riduzioni della dose da 10% a 60% con valore medio di 22 – 28% [11].
Figura 1.9 : modulazione angolare [9]
Nella tabella 1.4 sono riportati i sistemi di ATCM attualmente disponibili su tomografi a 16 strati.
Ditta produttrice | Nome | Livello di controllo automatico dei mA | Prescrizione dei mA | Calcolo dell’attenuazione |
GE | SmartmA |
| Indice di rumore specificato dall’utente |
|
Philips | DoseRight ACS e DOM |
| Immagine di riferimento con livello di rumore desiderato specificato dall’utente |
|
Siemens | CAREDose 4D |
| mAseff per un paziente standard specificato dall’utente |
|
Toshiba | SUREExposure |
| Indice di dose specificato dall’utente |
|
Tabella 1.4 : tecniche di modulazione della corrente nel tubo per tomografi a 16 strati [8]
Il tomografo ideale dovrebbe disporre di entrambi i sistemi per garantire il massimo dell’efficacia.
La modulazione automatica della corrente nel tubo richiede una conoscenza delle caratteristiche di attenuazione del paziente che si possono ricavare a partire da una scout del paziente. Per quanto riguarda la modulazione nel piano x-y, è possibile ottenere le informazioni necessarie per variare i mA in due modi: o si utilizzano i dati della scout view per calcolare le dimensioni antero-posteriori e latero-laterali del paziente in ogni rotazione e i mA vengono modificati sinusoidalmente in modo da adattarsi a tali parametri, oppure si sfruttano online i dati dai 180° precedenti nella rotazione per modulare i mA.
Quando si utilizzano le tecniche di ATCM bisogna adottare dei metodi per selezionare il livello di qualità dell’immagine desiderato; a tale scopo sono possibili diversi approcci. Su alcuni sistemi vengono dati come input i mA che verrebbero utilizzati senza modulazione, e questo valore costituisce la “linea di base” per calcolare i mA necessari per ottenere lo stesso livello di rumore per diverse dimensioni del paziente. Altri sistemi richiedono come input un indice di qualità dell’immagine, che è solitamente legato ad un valore di rumore; i mA vengono regolati in modo da mantenere questo livello di rumore per tutte le sezioni del paziente. Infine, un terzo approccio consiste nel selezionare una “immagine di riferimento” che abbia le caratteristiche di qualità richieste per un determinato esame; questa immagine è poi utilizzata per adattare i mA in modo che venga raggiunto lo stesso livello di qualità per ogni paziente.
In alcuni casi è possibile impostare i limiti superiore e inferiore di mA che possono essere utilizzati dal sistema di ATCM.
La modulazione della corrente nel tubo, oltre che ad essere un metodo efficace di riduzione della dose, può essere di beneficio per la qualità dell’immagine, perché permette di ottenere una qualità delle immagini consistente da paziente a paziente, da strato a strato e infine all’interno dello stesso strato. La modulazione nel piano x-y contribuisce inoltre a ridurre gli artefatti a strisce causati da un basso flusso di fotoni nelle proiezioni laterali di regioni anatomiche come le spalle e la pelvi. Infine tali tecniche permettono di diminuire il carico al tubo radiogeno allungandone il tempo di vita media [8]
2 FANTOCCI PER LA VALUTAZIONE DELLE IMMAGINI TCMS
Questo capitolo contiene una descrizione degli oggetti test necessari per effettuare le valutazioni sulle apparecchiature tomografiche. Lo scopo prefissato è quello di mettere in luce i limiti degli oggetti test oggi disponibili per gli apparecchi di ultima generazione e di offrire una guida all’acquisto del materiale necessario per la caratterizzazione di un sistema TCMS.
2.1 Fantocci specifici per la qualità immagine
Gli oggetti test da utilizzarsi per la qualità immagine sono cilindri in materiale plastico che contengono acqua; in alternativa possono essere costituiti da “acqua solida” (in genere PMMA) che ha caratteristiche di attenuazione simili all’acqua (numero TC = 0 ± 5 HU) ma si presenta più stabile e non crea problemi legati allo riempimento e alla fuoriuscita del fluido. Il diametro del cilindro è compreso tra 15 a 25 cm, a seconda che simuli solo la testa, solo il corpo o una via intermedia.
Spesso si presentano come oggetti multistrato dove ogni strato contiene gli inserti necessari per le specifiche valutazioni.
Si tratta di uno strato senza inserti riempito di acqua o materiale uniforme.
Il rumore dell’immagine dipende dalle dimensioni del fantoccio e dalla sua composizione. Di solito, i fantocci impiegati per la misura del rumore hanno forma cilindrica e sono riempiti d’acqua, oppure sono costituiti di un materiale omogeneo equivalente all’acqua. Il fantoccio deve essere centrato rispetto al campo di vista (FOV).
Un fantoccio di grandi dimensioni può essere impiegato per FOV grandi (protocolli body), mentre un fantoccio piccolo, dotato di un anello esterno per simulare la presenza dell’osso corticale, è indicato per valutare i protocolli specifici per l’encefalo. Fantocci ellittici possono essere impiegati per valutare gli effetti sul rumore prodotti da parte dei sistemi di riduzione della dose che modulano la corrente nel tubo in funzione dell’attenuazione prodotta dall’oggetto in esame.
Spesso i tomografi hanno in dotazione un fantoccio per i controlli di qualità e, talvolta, è disponibile una serie di fantocci che viene utilizzata dai tecnici incaricati della manutenzione per la calibrazione dei diversi campi di vista. Impiegando il fantoccio con il diametro maggiore, si analizza il campo di vista massimo e, allo stesso tempo, si controllano tutti gli elementi rivelatori verificando la presenza di artefatti ad anello.
L’inserto utilizzato è un foglio o un filo ad alta densità (ad esempio alluminio) inclinato lungo z con un angolo compreso comunemente tra 23° e 45°. Per valutazioni di strati di spessore inferiore a 2 mm, lo spessore dell’inserto e l’angolo di inclinazione possono diventare critici; in questi casi occorre scegliere gli oggetti con rampa più sottile e con inclinazioni minori. Lo spessore minimo che può essere misurato dipende dallo spessore T della rampa d’alluminio e dall’angolo θ d’inclinazione :
(2.1) smin = T / cos(θ )
Nel caso di spessori molto sottili, ad esempio 0.5 mm, è necessario utilizzare una rampa con un’inclinazione di circa 5° che permette un’amplificazione del profilo di circa un fattore 10 (amplificazione = (tangθ)–1); contemporaneamente la rampo non può superare 0,5 mm: in queste condizioni è possibile campionare correttamente lo spessore dello strato.
A tutt’oggi esistono pochi fantocci con queste ultime caratteristiche, ma è possibile facilmente costruirne con semplici mezzi [12]. Un fantoccio in commercio che sembra superare queste difficoltà è il modulo 591 CTP del CatPhan che dispone di 4 rampe inclinate di 26° che coprono 4 cm di lunghezza per gli spessori più ampi dei tomografi multistrato e 2 rampe inclinate di 7° che coprono 6.25 mm per gli spessori molto sottili; le rampe sono costituite da piccole sfere di tungsteno di 250 µm di diametro nel primo caso e 180 µm nel secondo. Il gruppo Impact, inoltre, ha sviluppato un fantoccio con una rampa in titanio di spessore 50 µm e inclinato di 5° rispetto al piano di scansione.
Figura 2.1: schema modulo 591 CatPhan 600 per misura spessori di strato – MTF e SSP[35]
Un altro aspetto estremamente critico per le TCMS è la lunghezza dell’inserto lungo l’asse z che deve coprire la massima estensione del fascio per consentire l’acquisizione simultanea di tutti gli strati possibili nella configurazione più ampia.
Nel caso delle TCMS si è riscontrata una criticità nella posizione delle rampe all’interno del fantoccio : nel caso di posizioni periferiche la valutazione risente di artefatti da conebeam reconstruction rendendo impossibile una corretta misura.
Come noto, nei tomografi spirale la misura dello spessore dello strato ricostruito non può essere effettuata utilizzando il metodo della rampa inclinata, ma, utilizzando un fantoccio dedicato. Questo può essere costituito da una sferetta o, in alternativa, da un disco sottile (< 0.1 mm) di materiale ad alta densità (PTFE politetrafluoroetilene, oro, tungsteno) sostenuto da un mezzo di densità più bassa (spugna o Perspex)
Nella seguente tabella 2.1 sono riportate le caratteristiche di tre fantocci per la misura dell’SSP disponibili in commercio.
Marca | materiale | Fondo | dimensioni (µm) |
QRM | foglio d’oro | plastica equivalente | 25 |
CatPhan – CTP 528 | sfera tungsteno | mezzo solido (≈ 90 n.TC) | 280 |
AAPM | sfera acciaio | Spugna | 250 |
Tabella 2.1 Caratteristiche dei fantocci in commercio per la misura della SSP
Quasi tutti i fantocci dedicati ai controlli di qualità delle apparecchiature tomografiche, dispongono di pattern ad alta densità (differenza di almeno 100 n. TC) con frequenza variabile. Le frequenze utili vanno da 1-4 cpl/cm fino a 12- 15 cpl/cm, consentendo di caratterizzare adeguatamente la curva MTF con il metodo di Droege [13] anche se non permettono di visualizzare le frequenze spaziali limite dei nuovi sistemi tomografici che possono raggiungere con filtri dedicati le 21 – 25 cpl/cm.
Figura 2.2 Esempio di oggetto test con dettagli a frequenza spaziale variabile [20]
In alcuni casi il pattern viene collocato radialmente per ridurre gli artefatti a striscia.
In altri casi al pattern a onda quadra si preferisce il pattern costituito da cilindri cavi, utile solo per valutazioni visive.
In aggiunta a quelli già descritti, alcuni fantocci contengono inserti come gradini inclinati (edge), fili sottili e sferette metalliche inseriti in un substrato omogeneo per permettere il calcolo della MTF con i metodi della edge spread function (ESF), della line spread function (LSF) o della point spread funcion (PSF) rispettivamente.
A fianco dei fantocci che consentono la misura della risoluzione spaziale nel piano ricostruito, può essere utile la misura della risoluzione spaziale lungo l’asse z, parametro che caratterizza la qualità delle ricostruzioni multiplanari e volumetriche. Il valore limite per questo parametro è attualmente pari a 14 cpl/cm. Un fantoccio in commercio ideato per questo scopo è il QRM 3D Spatial Resolution Test Phantom: è costituito da due spessori in plastica con pattern a fori di diametro da 4 mm a 0.4 mm corrispondenti alle frequenze spaziali comprese tra 1.25 cpl/cm e 12.5 cpl/cm. I due spessori sono ortogonali e opportunamente posizionati permettono la valutazione (visiva) della risoluzione massima nel piano assiale e lungo z (piano sagittale e coronale).
Figura 2.3 QRM 3D Spatial Resolution Test Phantom [33]
La scelta dei materiali utili per caratterizzare l’attenuazione e quindi la scala dei n. TC, è varia: polietilene, acrilico (plexiglass), polistirene, nylon, policarbonato, teflon.
I fantocci contengono generalmente alcuni di questi inserti: l’intervallo dei n. TC abbinati deve però essere indicato dalla Ditta costruttrice del tomografo perché dipende dalla qualità della radiazione cioè dalla tensione, dallo spettro energetico e dalla filtrazione del fascio radiante. Nella tabella 2.2 sono riportati per i principali materiali presenti nei fantocci, dati di densità, di densità elettronica, oltre che il fattore F per diversi valori di energia efficace della radiazione, dove F è il rapporto tra i coefficienti di attenuazione massici del materiale in questione rispetto a quello dell’acqua. Questi valori possono essere utili nel caso di utilizzo delle immagini per la preparazione di piani di trattamento radioterapico, qualora mancassero dati certificati relativi al fantoccio utilizzato. In particolare il numero TC dell’alluminio o del magnesio si prestano a determinare il valore di energia efficace della radiazione perché più sensibili all’energia del fascio a causa del valore di Z più alto rispetto ai materiali tessuto equivalente.
Materiali o Tessuti | Densità (g/cm3) | e-/g (x10E-23) | e-/cm3 (x 10E-23) | e-/cm3 (relativo) | Rapporto F | |||
60 keV | 70 keV | 80 keV | 100 keV | |||||
Aria | 0.0010 | 3.0060 | 0.0030 | 0.0009 | 0.9033 | 0.9023 | 0.9011 | 0.8927 |
Polmone equivalente | 0.2400 | 3.2860 | 0.7886 | 0.2359 | 0.9033 | 0.9023 | 0.9011 | 0.8927 |
Grasso | 0.9160 | 3.3400 | 3.0594 | 0.9151 | 0.9603 | 0.9743 | 0.9806 | 0.9871 |
Polietilene (C2H4) | 0.9500 | 3.3400 | 3.1730 | 0.9491 | 0.9550 | 0.9800 | 0.9924 | 1.0010 |
Acqua (H2O) | 1.0000 | 3.3433 | 3.3433 | 1.0000 | 1.0000 | 1.0000 | 1.0000 | 1.0000 |
Polistirene (C8H8) | 1.1100 | 3.2430 | 3.5997 | 1.0767 | 0.9057 | 0.9270 | 0.9429 | 0.9502 |
Acqua solida | 1.0300 | 3.3343 | 3.4343 | 1.0272 | 1.0000 | 1.0000 | 1.0000 | 1.0000 |
Tessuto molle | 1.0400 | 3.4200 | 3.5568 | 1.0639 | 0.9962 | 0.9930 | 0.9923 | 0.9915 |
Nylon (C6H11NO) | 1.1100 | 3.3200 | 3.8180 | 1.1420 | 0.9365 | 0.9537 | 0.9619 | 0.9702 |
Policarbonato (C16H14O3) | 1.1900 | 3.1770 | 3.7806 | 1.1308 | 0.9061 | 0.9197 | 0.9239 | 0.9302 |
Acrilico (C5H8O2) | 1.1800 | 3.2480 | 3.8326 | 1.1464 | 0.9291 | 0.9395 | 0.9500 | 0.9608 |
Bakelite (C43H38O7) | 1.2500 | 3.1790 | 3.9738 | 1.1886 | 0.9049 | 0.9202 | 0.9261 | 0.9384 |
Carbone | 2.2500 | 3.0080 | 6.7680 | 2.0243 | 0.8495 | 0.8657 | 0.8750 | 0.8850 |
Teflon (C2F4) | 2.2140 | 3.0110 | 6.6664 | 1.9939 | 0.9117 | 0.8983 | 0.8927 | 0.8808 |
Magnesio | 1.7380 | 2.9905 | 5.1975 | 1.5546 | 1.2475 | 1.1295 | 1.0598 | 0.9906 |
Osso (Compatto) | 1.8500 | 3.1920 | 5.9052 | 1.7663 | 1.5088 | 1.3219 | 1.2045 | 1.0869 |
Osso equivalente | 1.9330 | 3.0800 | 5.9536 | 1.7808 | 1.5088 | 1.3219 | 1.2045 | 1.0869 |
Alluminio | 2.6990 | 2.9020 | 7.8325 | 2.3427 | 1.3520 | 1.1975 | 1.1031 | 1.0000 |
Tabella 2.2: Valori di densità, densità elettronica e F per vari materiali ed energie efficaci [46].
Qualora le immagini TC debbano essere inviate ad un sistema di Treatment Plannig per la pianificazione di un trattamento radioterapico, è necessario conoscere la corrispondenza esatta tra n. TC e densità elettronica per permettere al sistema TP la accurata correzione per le disomogeneità. Per questa valutazione sono disponibili in commercio oggetti test specifici (Electron Density CT Phantom) che dispongono di numerosi dettagli. Tra i fantocci più noti e diffusi c’è il Modello 467 Gammex-RMI e il Modello 62 CIRS rappresentati nella figura 2.4. La relazione tra n. TC e densità elettronica è approssimativamente lineare, anche in corrispondenza dei valori TC alti presenta una deviazione a causa al contributo elevato dell’effetto fotoelettrico all’attenuazione rispetto all’effetto Compton.
(a) (b)
(c)
Figura 2.4 Electron Density Phantom (a) (c) [42], (b) [36]
La risoluzione a basso contrasto viene caratterizzata utilizzando oggetti a basso contrasto rispetto al materiale in cui sono immersi; i contrasti utili vanno da 0.3 %, 0.5 %, 1 %, 2% (corrispondenti a differenze in n.TC di 3, 5, 10, 20) e le dimensioni utili dei diametri degli inserti vanno da 2 a 10-15 mm. Per le apparecchiature TCMS si tenga conto che la dimensione lineare dell’inserto dovrebbe coprire la massima ampiezza dei rivelatori (almeno 4 cm). L’oggetto che in commercio più corrisponde a queste esigenze è il modulo 515 del CatPhan. Esistono tuttavia altri oggetti con queste caratteristiche (Diagnostic Imaging Model 76-409 (CIRS), Gammex 464, Elimpex ). Altri oggetti richiedono invece di essere riempiti con soluzioni idonee, comportando per questo problemi pratici, come l’inserto ATS del fantoccio AAPM.
Altri ancora sono costruiti con un sottile foglio di polietilene contenenti fori: è chiaro che questi ultimi oggetti non sono idonei alla misura in acquisizione spirale, e presentano problemi di allineamento anche per le apparecchiature multistrato. Si ricorda infine, che nella letteratura sono anche proposti in via sperimentale oggetti test per la valutazione del basso contrasto in 3 dimensioni [2, 14].
(a) (b)
(c)
Figura 2.5 Esempio di alcuni fantocci per la valutazione del basso contrasto : a) CatPhan 500 [15] b) Gammex 464 [15], c) Diagnostic Imaging Model 76-409 (CIRS) [36]
Non esistono oggetti standard per la valutazione degli artefatti da Cone Beam. Per natura, gli artefatti si presentano in corrispondenza di oggetti situati in posizione periferica rispetto all’asse di rotazione e su oggetti di forma o dimensioni non costanti lungo l’asse z.
Tra le proposte commerciali che possiamo menzionare c’è il Clock Phantom prodotto su ordinazione dalla Ditta QRM, in cui sfere di PTFE di diametro pari a 3 o 1.5 cm sono posizionate all’interno di un cilindro nella posizione delle ore di un quadrante di orologio.
Figura 2.6 – Schema del Clock Phantom [33]
In alternativa con metodi artigianali è possibile realizzare in loco fantocci utili alla valutazione degli artefatti di cui sopra [15], oppure è possibile utilizzare fantocci non dedicati (modulo 401 CTP).
Figura 2.7 – Esempio di fantoccio casalingo [15] o di utilizzo del CatPhan
2.2 Misure dosimetriche: strumentazione e fantocci
Per la misura degli indici di dose quali il CTDI e il DLP è necessario dotarsi di una camera a ionizzazione di tipo pencil (stilo), ovvero con una camera a forma cilindrica di lunghezza sensibile di 10 cm e di diametro circa 1 cm con un volume sensibile di circa 3 cm3. E’ fondamentale che questi strumenti abbiano una risposta uniforme su tutta la lunghezza. In generale sono calibrati in kerma in aria mediante esposizione a un campo RX uniforme. Nella scelta della qualità del fascio da utilizzare per la calibrazione è consigliabile scegliere un fascio di HVL1 tra 7 e 10 mm di Al [49]. Si tratta di strumenti che si adattano a diversi tipi di elettrometri; in alcuni casi si trovano in commercio camere con lunghezza sensibile superiore (es: 14 cm). Dal momento che la grandezza dosimetrica oggi di riferimento è il CTDI100, per semplificare la valutazione è più opportuno acquistare direttamente uno strumento che effetti l’integrazione su 10 cm. Nell’utilizzare la lettura dell’elettrometro occorre verificare (dalla documentazione o sperimentalmente) se la lettura dell’elettrometro è in integrale (Gy × cm) o se è già divisa per la lunghezza della camera.
E’ possibile eseguire misure di CTDI e DLP anche con dosimetri a termoluminescenza; i TLD devono essere opportunamente calibrati con un fascio radiante con caratteristiche simili a quelle del tomografo e deve essere riprodotta la geometria di irradiazione più idonea alla misura da eseguire.
Per effettuare le misure in fantoccio si utilizzano il fantoccio HEAD o quello BODY.
Il fantoccio HEAD è costituito da un cilindro di PMMA di 16 cm di diametro e di 15 cm di lunghezza con un foro centrale e 4 fori nelle posizioni corrispondenti a ore 12, 3, 6, 9 utilizzabili come alloggiamenti per la camera a ionizzazione; i quattro alloggiamenti non utilizzati dalla camera, devono essere sempre riempiti con cilindri rimuovibili di PMMA. Il fantoccio BODY ha le stesse caratteristiche del fantoccio HEAD, ma diametro di 32 cm.
Figura 2.8 – Esempio di fantoccio HEAD
Esistono in commercio fantocci per misure in campo pediatrico: le caratteristiche sono simili a quelle dei fantocci utilizzati per il paziente adulto ma il diametro del fantoccio HEAD PEDIATRICO misura 10 cm e il fantoccio BODY PEDIATICO ha un diametro di 16 cm .
Un nuovo tipo di rivelatore (CT-SD16) è proposto dalla ditta RTI Electronics AB : si tratta di una sonda cilindrica in cui sono presenti due rivelatori semiconduttori molto piccoli (250 μm). I due rivelatori, posizionati in aria libera o in fantoccio, registrano il profilo di dose durante un’acquisizione con movimento continuo del lettino (acquisizione spirale). Il CTDI100 si può misurare così integrando il profilo di dose così ottenuto. Da questo tipo di misura possono essere ricavate altre informazioni relative al movimento del lettino, al profilo di dose, e all’attenuazione del supporto del paziente.
Figura 2.9 – Sonda CT-SD16 RTI Electronics [43]
3 PARAMETRI DI QUALITA’ DELL’IMMAGINE
Le seguenti sezioni sono dedicate alla valutazione della qualità di un’immagine transassiale. In generale, si considera che l’immagine sia stata acquisita in modalità sequenziale. In ciascuna sezione, un paragrafo descrive i diversi criteri e metodi richiesti per le immagini assiali acquisite in modalità spirale. In un altro paragrafo sono invece discussi i procedimenti specifici per la tecnologia multistrato, in modalità di acquisizione sia assiale che spirale.
3.1 Rumore
Anche le immagini TC, come quelle prodotte da altre modalità di imaging, sono affette da rumore. Il rumore d’immagine si manifesta come oscillazioni dei numeri TC di un oggetto omogeneo intorno a un valore medio. Oltre a ciò, possono essere presenti altre variazioni, chiamate rumore strutturale o artefatti. A rigore, il rumore dovrebbe essere misurato a partire da una serie di scansioni di un determinato oggetto, sempre nelle medesime condizioni. Tuttavia, un approccio più pratico consiste nell’esprimere il rumore in termini di deviazione standard normalizzata relativa a un insieme di numeri TC misurati al centro di un’immagine di un oggetto omogeneo. Questa misura della varianza del campione include il contributo da altri fattori in aggiunta al rumore casuale o quantico, quali il rumore elettronico o il rumore strutturale.
Per eseguire un confronto diretto tra apparecchiature TC con diverse scale di contrasto, è indispensabile calcolare la deviazione standard normalizzata (S):
(3.1)
dove:
σacqua è la deviazione standard dei valori dei pixel compresi nella ROI selezionata sull’immagine di un oggetto omogeneo
TCscala = TCacqua – TCaria
TCacqua e TCaria sono i valori del numero TC rispettivamente dell’acqua e dell’aria.
Se espressi in unità Hounsfield, il numero TC dell’acqua e quello dell’aria sono uguali, per definizione, rispettivamente a zero e a -1000. Alcune case costruttrici, tuttavia, dimezzano l’intervallo dei numeri TC per particolari modalità ad alta risoluzione, e questo può arrecare confusione qualora non venga data indicazione all’utilizzatore.
La deviazione standard normalizzata percentuale coincide con la definizione secondo l’AAPM, σuw%, a patto che sia lineare l’andamento della scala TC in funzione del coefficiente di attenuazione lineare.
La deviazione standard è misurata in una ROI ragionevolmente piccola; si possono utilizzare aree maggiori nell’ipotesi che si possa escludere la presenza di rumore strutturale o di disomogeneità nella parte di immagine in esame. La norma CEI 62-135 [38] specifica che il diametro sia pari al 40% del diametro del fantoccio. Quando siano impostati diversi field of view (FOV), si raccomanda di modificare le dimensioni della ROI in modo che essa contenga sempre la medesima area.
Se è possibile effettuare la sottrazione d’immagine, allora il rumore strutturale può essere eliminato misurando il rumore dell’immagine ottenuta per sottrazione da due immagini acquisite in modo identico. Il valore così ottenuto deve essere diviso per per consentirne il confronto con il rumore stocastico relativo a una singola immagine.
Sebbene elimini ogni rumore strutturale, questo metodo presuppone la costanza delle prestazioni dell’apparecchiatura. Per tomografi senza la modalità spirale, si dovrebbero utilizzare scansioni alternate, in quanto ci possono essere piccole variazioni nelle caratteristiche dell’immagine dipendenti dalla direzione di rotazione del tubo, che cambia con le acquisizioni alternate. La sottrazione di immagine può essere inappropriata per le immagini acquisite in modalità spirale, a causa della dipendenza del rumore dalla posizione lungo l’asse z dell’immagine ricostruita rispetto alla posizione del tubo.
Per calcolare TCscala, è possibile ricreare un volume d’aria posizionando al centro del fantoccio omogeneo un inserto di almeno 20 pixel di diametro riempito d’aria. Il valore del numero TC dell’acqua e dell’aria è dato dal valore medio calcolato all’interno di una piccola area. Alternativamente, all’aria è generalmente attribuito un numero TC uguale a -1000 e, per un rapido controllo, può essere utilizzata una zona d’aria appena al di fuori del fantoccio. Questo metodo è valido purché non sia stata effettuata una compressione dei dati dell’immagine per cui i valori dei pixel prossimi a quello dell’aria sono stati artificialmente posti uguale a -1024 (il minimo valore possibile per molti tomografi).
I valori del rumore misurati da scansioni successive della stessa regione del fantoccio possono mostrare una variazione del 15%. Pertanto, per avere una stima accurata del rumore, si dovrebbero acquisire almeno dieci immagini e calcolare la media dei valori di rumore ottenuti.
Le misure di rumore sulle immagini ottenute per mezzo di un’acquisizione spirale sono effettuate con le stesse modalità delle acquisizioni assiali. Occorre comunque assicurarsi, per non introdurre errori, che la lunghezza dell’irradiazione effettuata per ricostruire l’immagine copra soltanto la parte del fantoccio contenente uniformemente acqua e non altri inserti presenti nel fantoccio. Per questo è possibile acquisire tutto il fantoccio in modalità spirale e effettuare la misura sullo strato centrale corrispondente all’inserto uniforme.
I fantocci che non sono stati appositamente concepiti per l’acquisizione spirale potrebbero non essere sufficientemente lunghi; in questi casi, è consigliabile impostare un pitch uguale a 1 per uno spessore dello strato pari a 5 mm; con pitch maggiori, si dovrebbe selezionare uno spessore di strato più sottile.
La costanza dei valori di rumore nella regione perimetrale dell’immagine del fantoccio dipende dalla posizione lungo l’asse z dell’immagine ricostruita [17]. Questa posizione è correlata alla posizione angolare assunta dal tubo durante la scansione. L’effetto è comunque minimo per gli algoritmi di interpolazione che agiscono su 360°. Anche le misure effettuate all’isocentro possono mostrare questa variazione se il fantoccio è stato posizionato sul lettino e il lettino produce una certa attenuazione.
La variazione del valore del rumore da un’acquisizione assiale a una spirale, qualora sia utilizzato lo stesso algoritmo di ricostruzione sul piano di scansione, dipende dall’algoritmo di interpolazione lungo z adottato e può essere nota a priori per l’usuale algoritmo di interpolazione lineare [17]: l’algoritmo di interpolazione lineare che ricostruisce utilizzando i dati di 360° produce un rumore minore di circa il 18% rispetto alla modalità di acquisizione assiale standard, mentre l’algoritmo di interpolazione lineare che agisce su 180°, un rumore maggiore di circa il 12%. Per algoritmo di interpolazione di ordine superiore il valore dato è specifico per quel particolare algoritmo. I valori di rumore misurati sull’immagine acquisita in modalità spirale con un’apparecchiatura a singolo strato non variano al variare del pitch [17] Si suggerisce durante le prove di accettazione dell’apparecchiatura di misurare il rumore per acquisizioni spirali con tre valori di pitch (indicativamente pari 0.5 – 1 – 1.5 ) e di valutarne il rapporto rispetto a un’acquisizione assiale di uguali parametri per verificarne la specifica dipendenza.
Le caratteristiche del rumore nella tecnologia multistrato dovrebbero essere considerate separatamente nelle due modalità di acquisizione assiale e spirale. La valutazione in modalità assiale permette di verificare che i rivelatori paralleli operino a parità di sensibilità. In modalità spirale, invece, tutti i banchi di rivelatori possono contribuire alla produzione dell’immagine finale.
Per verificare che i banchi di rivelatori abbiano la stessa sensibilità, si esamina il fantoccio in modalità assiale e si misura il rumore sulle immagini ottenute da ciascun strato. Come per i tomografi a singolo strato, si dovrebbero acquisire un certo numero di immagini della parte omogenea del fantoccio (per esempio dieci), al fine di poter calcolare il valore medio del rumore
Se i banchi dei rivelatori danno differenti valori medi di rumore ciò potrebbe significare che i banchi hanno diversa sensibilità, oppure che il sistema di collimazione non è centrato rispetto al piano di scansione, così da creare una disparità di irradiazione fra i due banchi di rivelatori più esterni.
Se vengono utilizzate diverse combinazioni di rivelatori, e se i difetti di collimazione dipendono dallo strato occorrerebbe valutare tutte le combinazioni di spessore dello strato.
A causa del diverso metodo utilizzato per la ricostruzione dell’immagine nella modalità spirale con sistemi multistrato la relazione tra rumore d’immagine e pitch è differente rispetto alla tecnologia a strato singolo.
Nella tecnologia a singolo strato, all’aumentare del pitch il rumore d’immagine non varia; questo è dovuto al fatto che la ricostruzione dell’immagine si basa sull’interpolazione generalmente di due proiezioni per ciascun angolo di rotazione, posizionate su ciascun lato del piano relativo all’immagine da ricostruire.
Nella tecnologia multistrato, un metodo comune è quello di utilizzare qualsiasi proiezione che sia entro una certa distanza lungo l’asse z dal piano di interesse. Questa flessibilità è possibile in quanto, disponendo di un certo numero di banchi di rivelatori, si hanno molte proiezioni per ciascun angolo di rotazione. Mantenendo fissa la distanza all’interno della quale vengono selezionate le proiezioni per l’interpolazione, lo spessore dello strato visualizzato rimane approssimativamente costante al variare del pitch. Tuttavia, le variazioni del pitch modificano il numero totale delle proiezioni o del campionamento dei dati utilizzati per ricostruire l’immagine tanto da influenzare il rumore. Per esempio, all’aumentare del pitch, si utilizzano campioni con un minor numero di dati per produrre l’immagine finale, e pertanto il rumore aumenta. Molti costruttori compensano automaticamente aumentando i mA, in modo che il rumore rimanga costante all’aumentare del pitch.
Come per il caso a singolo strato, si suggerisce durante le prove di accettazione dell’apparecchiatura di misurare il rumore per acquisizioni spirali con tre valori di pitch (indicativamente pari 0.5 – 1 – 1.5 ) e di valutarne il rapporto rispetto a un’acquisizione assiale di uguali parametri per verificarne la specifica dipendenza.
3.1.5 Condizioni operative
Il rumore dell’immagine è influenzato da molti parametri di scansione, e in questo senso è un ottimo test di valutazione delle prestazioni dell’apparecchiatura a parità di impostazioni.
I parametri che influiscono sul rumore sono: la tensione (kV), la corrente (mA) e il tempo di scansione (mAs), la filtrazione del fascio, il numero di campionamenti angolari per immagine, lo spessore dello strato, l’algoritmo di ricostruzione, il filtro immagine, la rotazione in senso orario piuttosto che in senso anti-orario per i tomografi privi dei contatti striscianti, la posizione dell’immagine lungo l’asse z per le acquisizioni spirali, le dimensioni della macchia focale.
L’andamento del rumore quantico d’immagine soddisfa alla seguente relazione:
(3.2)
dove N indica il numero di fotoni che contribuiscono alla formazione dell’immagine. Sostanziali differenze rispetto a questo andamento sono dovute ad altre cause, tra cui la presenza di rumore elettronico.
Dal momento che sono molti i parametri di scansione che influiscono sul rumore, risulta assai complesso determinare i valori di riferimento per ciascuna combinazione dei parametri di scansione. Pertanto, per controlli di routine, è necessario fare una scelta relativamente al protocollo di acquisizione da utilizzare. In fase di accettazione, si dovrebbero impostare i protocolli clinici più comunemente utilizzati. Per le prove di funzionamento, possono essere scelti uno o due protocolli, oppure possono essere esaminati a rotazione a seconda dell’utilizzo.
3.1.6 Dispositivo di prova
Per la descrizione dei dispositivi di prova si rimanda al capitolo relativo ai fantocci per la valutazione della qualità in TCMS.
Si raccomanda solo, durante i test di accettazione, di utilizzare lo stesso fantoccio con il quale è stata effettuata la misura del rumore durante la calibrazione o durante la verifica in fabbrica poiché il rumore d’immagine dipende dalle dimensioni del fantoccio e dalla sua composizione. Al fine di determinare i valori di riferimento, è necessario utilizzare lo stesso fantoccio che verrà impiegato per i controlli periodici. Per tali controlli, è ottimale utilizzare uno dei fantocci in dotazione dell’apparecchiatura o un fantoccio di facile reperibilità.
3.2 Risoluzione spaziale
3.2.1 Definizione e discussione
La risoluzione spaziale nel piano dell’immagine tomografica (piano tomografico) descrive la capacità di distinguere piccoli dettagli ad alto contrasto.
La risoluzione può essere determinata sia soggettivamente che quantitativamente. Può essere determinata in modo soggettivo, osservando l’immagine di una serie regolare di barre o bacchette ad alta risoluzione, oppure in modo quantitativo direttamente dalla point spread function (PSF) o dall’edge spread function (ESF). Queste funzioni sono calcolate a partire dall’immagine di una sferetta, di un filo metallico allineato lungo l’asse z o di un bordo ad alta risoluzione. La funzione di trasferimento della modulazione (MTF) può essere calcolata dalla PSF o dalla ESF e fornisce un’analisi numerica del contenuto in frequenze dell’immagine di un bordo o di un punto. Solitamente vengono confrontati i valori di frequenza ai quali la curva della MTF scende al 50% e al 10% .
Sebbene in teoria si possa utilizzare anche il metodo della misura della line spread function (LSF), in pratica non esistono oggetti test con inserti di questo tipo.
Il calcolo della MTF dipende dalla possibilità di accesso ai dati numerici contenuti nel tomografo, oltre che a un appropriato programma di analisi. In tempi recenti, questo non rappresenta più un problema grazie all’avvento dello standard di trasferimento delle immagini DICOM e alla possibilità di installare speciali programmi sui personal computer.
3.2.2 Metodi
Metodo quantitativo
La point spread function (PSF) può essere calcolata direttamente acquisendo l’immagine di un filo ad alto contrasto o di una sferetta la cui sezione abbia un diametro dell’ordine, o minore, della risoluzione che deve essere valutata. L’allineamento del filo deve essere molto accurato, in modo da evitare che l’immagine risulti sfuocata. La sferetta non richiede particolare cura nell’allineamento, ma produce un segnale più basso nell’immagine a causa dell’effetto di volume parziale.
Per assicurare un buon rapporto segnale-rumore, si dovrebbe acquisire l’immagine impostando un elevato valore della corrente nel tubo e, quando si utilizza il filo, un ampio spessore dello strato. Impiegando la sferetta, lo spessore dello strato influisce sia sul segnale che sul rumore, cosicché è necessario stabilire quale sia lo spessore ottimale. E’ necessario utilizzare un Campo di Vista (FOV) sufficientemente piccolo, tale che la dimensione del pixel non influenzi la misura (ad esempio FOV=10-15 cm) [38].
La point spread function è completamente descritta sommando i profili dei numeri CT che intersecano ad ogni angolo l’immagine del filo o della sferetta. La risoluzione può essere caratterizzata direttamente dalla PSF, misurando la massima ampiezza a metà altezza (FWHM) e la massima ampiezza a un decimo d’altezza (FWTM).
La edge spread function può essere utilizzata per determinare la risoluzione spaziale; si misura dall’immagine di un bordo di un blocco di materiale posto in un fantoccio pieno d’acqua. Il materiale utilizzato può essere PMMA (Perspex), anche se non produce un contrasto particolarmente elevato e il rapporto segnale-rumore diventa troppo piccolo a causa delle scansioni ad alta risoluzione intrinsecamente più rumorose. Un materiale con un più alto numero TC quale il Teflon risulta più indicato, sebbene in questo caso gli artefatti da indurimento del fascio possano diventare un problema.
Per assicurare un buon rapporto segnale-rumore, si dovrebbe acquisire l’immagine impostando un elevato valore della corrente nel tubo. Per evitare che l’immagine del bordo risulti sfuocata, la base del blocco deve essere perpendicolare al piano tomografico.
Differenziando la ESF si ottiene la line spread function (LSF).
La MTF è data dal modulo della trasformata di Fourier della LSF o dell’integrale della PSF e descrive il trasferimento di tutte le frequenze nel piano dell’immagine.
I valori calcolati sono solitamente le frequenza alla quale la modulazione scende al 50% o al 10%. La forma della MTF dipende dal filtro di convoluzione utilizzato. Il limite visivo corrisponde a un livello della MTF compreso tra il 2% e il 5%. Questo limite non viene generalmente citato, dal momento che l’elevato rumore associato agli algoritmi di alta risoluzione comporta una maggior variazione statistica della MTF alle alte frequenze. La risoluzione limite dell’apparecchiatura è spesso indicata in corrispondenza dello 0%.
Metodo soggettivo
La valutazione soggettiva della risoluzione spaziale ad alto contrasto viene effettuata osservando le immagini di una serie regolare di barre o bacchette ad alta densità, con, rispettivamente, larghezza o diametro decrescente. Lo spazio tra le barre o le bacchette è uguale alla loro larghezza o diametro.
La risoluzione limite è valutata determinando fino a quale dimensione è possibile vedere la serie in modo nitido con tutti gli inserti chiaramente distinti. In alcuni fantocci, gli inserti sono in alluminio e si trovano inseriti in un fantoccio pieno d’acqua o costituito da un materiale equivalente all’acqua, oppure sono ottenuti semplicemente creando una cavità o un scanalatura in un materiale equivalente all’acqua.
Al fine di rendere riproducibile la valutazione qualitativa della risoluzione spaziale limite devono essere stabiliti i criteri di visualizzazione e devono essere standardizzate le condizioni di osservazione, quali l’illuminazione e il livello e l’ampiezza della scala dei grigi.
Metodo di Droege
Il metodo permette il calcolo di un limitato numero di punti di MTF attraverso l’utilizzo di semplici funzioni presenti in tutti i tomografi quali la media e la deviazione standard di una ROI. Il dispositivo di prova consiste di una serie di barre o bacchette di dimensioni decrescenti, separate da una distanza uguale alla loro larghezza o diametro. L’analisi di ciascun gruppo di barre o bacchette fornisce un valore, a una particolare frequenza, della curva della funzione di trasferimento della modulazione. Questo metodo è stato descritto da Droege e Rzeszotarski [13,18].
Un’immagine è ricostruita a partire dalle proiezioni acquisite lungo una certa porzione del fantoccio, ed è pertanto importante che questa porzione esaminata, alla quale appartengono le proiezioni usate per ricostruire l’immagine, copra per intero il dispositivo di prova.
La risoluzione nel piano di scansione, se misurata dall’immagine di un dispositivo di prova che è omogeneo nella direzione z, non è generalmente influenzata dalla modalità di acquisizione spirale; ciò si verifica, tuttavia soltanto se, in modalità volumetrica, si utilizza lo stesso kernel di convoluzione impiegato per la ricostruzione dell’immagine assiale.
Una piccola differenza nella risoluzione può risultare evidente quando il sistema della doppia proiezione (quarter detector shift), ottenuto mediante una configurazione meccanica per cui gli elementi del rivelatore sono costantemente disallineati rispetto all’asse centrale di un quarto della larghezza del rivelatore, è attivo nel modo assiale ma non in modalità spirale. Questa configurazione consente di ottenere un numero doppio di proiezioni, essendo il disallineamento pari a metà della larghezza del rivelatore, e quindi, considerando separatamente i campioni di dati, una risoluzione migliore.
In modalità assiale e spirale con tecnica multistrato, la procedura di analisi dell’immagine non si discosta da quanto già indicato. Si sottolinea che in MSTC è fondamentale che il dispositivo di prova si estenda oltre la lunghezza del volume acquisito, quando si impieghi un bordo o un filo e che l’utilizzo della sferetta limita l’analisi a una sola immagine.
La risoluzione spaziale nel piano di scansione è influenzata dal filtro di convoluzione impiegato per ricostruire l’immagine e da qualsiasi altro filtro di postelaborazione applicato. Dipende inoltre dal numero di proiezioni che compongono l’immagine. Questo numero dipende a sua volta dal rateo di campionamento e dal tempo di scansione. Queste dipendenze sono spesso più evidenti nelle immagini che sono ricostruite con algoritmi di risoluzione più elevata. Per esempio, la risoluzione limite di un tomografo spesso si ottiene con il tempo di rotazione più lungo, sebbene risoluzioni standard possano essere ottenute con tutti i tempi di scansione.
La misura della risoluzione spaziale dipende dal campo di vista ricostruito, dove la dimensione del pixel risultante corrisponde al valore limite. Per un corretto campionamento è necessario che le dimensioni del pixel siano inferiori dell’inverso del doppio della frequenza di cut-off prevista.
La risoluzione nel piano di scansione dipende inoltre dalle dimensioni della macchia focale; molti tomografi sono dotati di due macchie focali, che sono utilizzate in modo automatico in base alla scelta di determinati parametri di scansione.
Tecniche come quella che prevede di disallineare gli elementi del rivelatore rispetto all’asse centrale di un quarto della larghezza del rivelatore, o il dynamic focal spot (per cui la posizione della macchia focale oscilla tra due posizioni ogni pochi millisecondi) producono un numero doppio di proiezioni e pertanto forniscono una migliore risoluzione.
Un’altra tecnica che può essere impiegata è il collimatore “a pettine”, il quale si adatta sui rivelatori in modo da ridurre la loro larghezza effettiva e aumentare così la risoluzione spaziale dell’immagine.
Se il fantoccio è stato allineato in modo tale che il dispositivo di prova sia perpendicolare al piano di scansione, la risoluzione nel piano di scansione misurata è indipendente dallo spessore dello strato. L’allineamento del fantoccio non è particolarmente critico se si utilizza una sferetta ad alto contrasto.
La risoluzione spaziale nel piano di scansione è indipendente dai mA impostati. L’impiego di un’elevata corrente anodica e di uno spessore dello strato ampio, aumenta il rapporto segnale-rumore e consente un calcolo più corretto dell’MTF, minimizzando gli errori. Per garantire che le scansioni ad alta risoluzione utilizzino la macchia focale più piccola è necessario conoscere se l’apparecchiatura utilizza la macchia focale piccola solo per alcuni valori di mA o di spessore dello strato (strati sottili).
Normalmente, non si dovrebbe osservare una significativa variazione della risoluzione spaziale nel tempo. Alcune variazioni possono risultare evidenti nelle scansioni ad alta risoluzione a causa del deterioramento della macchia focale nel tempo.
Vi possono essere piccoli cambiamenti della risoluzione spaziale qualora si siano modificati i filtri di convoluzione durante un aggiornamento software .
In caso di significative sostituzioni di hardware, sarebbe opportuno verificare la risoluzione limite, dal momento che essa dipende da diversi fattori quali l’allineamento fuoco – rivelatore; se si utilizzano i collimatori del rivelatore per aumentare la risoluzione limite riducendo la larghezza effettiva del rivelatore, qualsiasi disallineamento andrà a modificare la risoluzione spaziale.
La risoluzione spaziale non è necessariamente uniforme attraverso il campo di vista e può decrescere allontanandosi dall’isocentro. Durante le prove di costanza, si dovrebbe valutare la risoluzione nella stessa posizione all’interno del campo di vista.
Per la descrizione dei dispositivi di prova si rimanda al capitolo relativo ai fantocci per la valutazione della qualità.
Si sottolineano, comunque, alcune caratteristiche peculiari dei diversi dispositivi di prova disponibili in commercio.
Il filo o la sferetta ad alto contrasto devono avere un diametro inferiore alla risoluzione che deve essere valutata.
La sferetta è l’unico inserto che non è soggetto ai problemi di allineamento ma genera un’immagine con un rapporto segnale-rumore ridotto. Gli altri dispositivi di prova devono essere correttamente allineati in modo che risultino paralleli al piano di scansione, perché altrimenti gli inserti diventerebbero effettivamente più larghi (barre, bacchette ecc.) o più sfuocati (bordo). L’impiego dei fantocci che utilizzano bacchette o barre in perspex immerse in acqua può risultare non idoneo alla valutazione degli algoritmi di più elevata risoluzione, in quanto il rumore può eguagliare la differenza in numeri TC. Questi fantocci, inoltre, devono essere esaminati periodicamente perché gli inserti in perspex possono distorcersi col tempo a causa dell’assorbimento di acqua da parte del materiale.
Per misurare la edge spread function, è necessario disporre di un fantoccio contenente un blocco di materiale ad alta densità a facce piane. Si considerano adeguate dimensioni dell’ordine di 80 × 40 mm nel piano dell’immagine e uno spessore che sia almeno il triplo dello spessore nominale dello strato irradiato. Il perspex può essere utilizzato per scansioni a bassa risoluzione; per le più elevate risoluzioni è più adatto un materiale di maggior densità quale il politetrafluoroetilene (PTFE).
3.2.8 Risoluzione lungo l’asse z
La risoluzione spaziale di una MPR (ricostruzione multiplanare) può essere valutata posizionando l’oggetto test (barre, cilindretti, bordi o fili di alto contrasto) orizzontalmente, lungo il piano parallelo al lettino. Si effettua poi una serie di acquisizioni assiali e si ricostruisce l’immagine nel piano coronale che passa per l’oggetto test. L’immagine ricostruita può quindi essere valutata nel solito modo. La risoluzione spaziale in questo piano dipenderà dallo spessore di strato e dall’incremento di ricostruzione del gruppo di immagini originali. Questo tipo di valutazione dovrebbe essere utile all’atto del commissioning per comprendere il funzionamento del sistema di ricostruzione MPR piuttosto che come test di routine.
3.3 n. TC e linearità
3.3.1 Definizione e discussione
Il numero TC (Hs) di un campione di un materiale s è definito dall’espressione
(3.3)
dove μs(E) e μw(E) sono i coefficienti di attenuazione lineare all’energia del fascio di raggi X rispettivamente del campione in esame e dell’acqua. K è una costante, che assume valore 1000 se il numero TC è espresso in unità Hounsfield, ma su alcuni apparecchi questo valore è dimezzato quando si utilizzano particolari algoritmi di convoluzione. Il processo di attenuazione in tomografia computerizzata è dominato dalle interazioni Compton per il tessuto molle, con qualche interazione fotoelettrica per materiali a più alto numero atomico (Z). Le interazioni Compton sono indipendenti dal numero atomico, proporzionali alla densità elettronica e inversamente proporzionali all’energia (E). L’effetto fotoelettrico è approssimativamente proporzionale a (Z/E)3.
Nella esecuzione dei piani di cura radioterapici, poiché l’effetto Compton è l’interazione predominante dei raggi X alle alte energie, deve essere stabilita la relazione tra la densità elettronica e il numero TC per la valutazione della distribuzione della dose in un’immagine TC.
3.3.2 Metodi di misura
Per valutare la relazione tra il numero TC e il coefficiente di attenuazione lineare, si acquisisce l’immagine di campioni di aria, acqua, Perspex, materiali equivalenti all’osso o qualsiasi altro materiale di composizione e densità nota inseriti in un apposito fantoccio. I coefficienti di attenuazione dei materiali dipendono dall’energia del fascio; sarebbe necessario conoscere lo spettro di energia dei raggi X, ma in prima approssimazione si può fare riferimento all’energia efficace del fascio, che alla tensione di 120 kV può essere assunta uguale a 70 keV. L’andamento del valori TC in funzione dei coefficienti di attenuazione lineare dovrebbe risultare una linea retta.
Per stabilire la relazione tra numeri TC e densità elettronica per i piani di cura radioterapici, si utilizza un fantoccio contenente inserti di densità elettronica nota. L’andamento dei numeri TC in funzione della densità elettronica è approssimativamente lineare, anche se in pratica devia dall’andamento lineare nella regione a più alti numeri TC a causa del maggior contributo delle interazioni fotoelettriche. Il valore del numero TC può variare da un’apparecchiatura all’altra, in dipendenza delle differenze nell’energia efficace.
Non vi sono indicazioni per eseguire questo controllo in modalità spirale. Qualora lo si effettui, occorre assicurarsi che i dati acquisiti provengano solo dal volume interno dell’inserto.
3.3.3 Condizioni operative
I valori dei numeri TC possono variare in seguito a ogni modifica allo spettro del fascio di raggi X e dovrebbero essere valutati per tutti i valori di tensione e per tutti i filtri impiegati. Possono inoltre variare con le dimensioni del campo e con gli algoritmi di ricostruzione.
Questo controllo è indispensabile, qualora l’apparecchiatura TC sia utilizzata in supporto alla radioterapia o per diagnosi basate sulla misura dei numeri TC.
3.3.4 Dispositivo di prova
Per la descrizione dei dispositivi di prova si rimanda al capitolo relativo ai fantocci per la valutazione della qualità in TCMS. I valori dei numeri TC possono essere influenzati dall’indurimento del fascio e sono pertanto sensibili alla forma, alle dimensioni e alla composizione del fantoccio.
3.4 Uniformità dei numeri TC
Un fantoccio riempito d’acqua dovrebbe fornire un’immagine uniforme a meno del rumore stocastico del sistema. Tuttavia, in pratica, scansioni di fantocci omogenei spesso mostrano graduali variazioni dei numeri TC attraverso l’immagine. Queste variazioni possono essere particolarmente visibili quando la parte omogenea del fantoccio è circondata da un materiale ad alto contrasto, quale quello che simula l’osso corticale.
Le valutazioni di questo parametro possono essere effettuate in modo quantitativo valutando l’andamento del profilo dei numeri TC attraverso l’immagine del fantoccio.
Un metodo semplice consiste nel calcolare il numero TC medio di una ROI al centro di una immagine di un fantoccio pieno d’acqua. Questo valore deve essere confrontato con quello relativo alle ROI situate in prossimità del bordo del fantoccio. Per confrontare apparecchiature diverse, la variazione massima del numero TC può essere espressa come percentuale della differenza tra i numeri TC dell’acqua e dell’aria:
(3.4)
dove
H1 = numero TC medio nella posizione centrale
H2 = numero TC medio nella posizione periferica
Hw = numero TC dell’acqua
Ha = numero TC dell’aria
In alternativa, può essere acquisito un profilo di numeri TC lungo il diametro del fantoccio. L’immagine di questo profilo, possibilmente correlata con i valori numerici dei singoli punti, può essere utilizzata come riferimento per le valutazioni successive. L’andamento dei profili può essere valutato visivamente oppure confrontando il valore assunto da un certo numero di punti prefissati.
3.4.3 Tecnica spirale
Il metodo sopra descritto può essere utilizzato su immagini di un fantoccio omogeneo acquisite in modalità spirale. Talvolta, vi possono essere grandi disuniformità con gli algoritmi di interpolazione su 180° e la posizione delle zone di disuniformità varia in funzione della posizione dell’immagine lungo l’asse Z rispetto alla posizione angolare del tubo RX.
In generale, le apparecchiature dispongono di algoritmi di correzione per l’indurimento del fascio che sono diversi a seconda della regione anatomica studiata.
L’uniformità spaziale di un fantoccio riempito omogeneamente d’acqua varia al variare della tensione e della filtrazione normalmente utilizzate. Può inoltre variare rispetto al numero delle posizioni angolari di campionamento, ai campi di vista di acquisizione e di ricostruzione, agli algoritmi di ricostruzione e ai programmi di retro-ricostruzione (post processing).
Questo parametro può variare in seguito a modifiche al software o all’hardware che vadano a modificare la filtrazione, gli algoritmi di indurimento del fascio ecc.
L’uniformità dei numeri CT, così come la linearità dei numeri CT, dipende dall’indurimento del fascio ed è sensibile alle dimensioni, alla forma e alla composizione del fantoccio. Questo parametro è di particolare importanza qualora l’analisi dei valori dei numeri CT venga utilizzata per finalità diagnostiche e, in questo caso, sarebbe opportuno utilizzare un idoneo fantoccio antropomorfo.
L’uniformità spaziale dipende dalle dimensioni e dalla composizione del fantoccio, particolarmente in presenza di materiali che simulano l’osso nei fantocci head, e in presenza di materiali di alto numero atomico.
Può essere utilizzato lo stesso fantoccio impiegato per valutare il rumore. Fantocci riempiti d’acqua costituiscono il materiale omogeneo adatto per questo tipo di controllo. Fantocci di piccole dimensioni (16 – 20 cm di diametro) e dotati preferibilmente di un inserto per simulare la presenza dell’osso sono indicati per le scansioni dedicate agli esami encefalici, mentre quelli di dimensioni maggiori (30 – 35 cm di diametro) sono adatti per i protocolli di scansione del corpo. Inoltre, si dovrebbero acquisire le immagini di un fantoccio di dimensioni maggiori, se disponibile, per garantire una buona uniformità per il più grande campo di vista.
Molti costruttori affermano che le loro apparecchiature sono calibrate per un particolare forma e dimensione del fantoccio. Sebbene molti fantocci per i controlli di qualità abbiano una sezione circolare, può essere appropriato utilizzare un fantoccio di forma ellittica.
3.5 Risoluzione a basso contrasto
3.5.1 Definizione e discussione
La sensibilità a basso contrasto è intesa come la capacità del sistema di distinguere oggetti di piccole dimensioni in un contesto di basso contrasto, quantitativamente di poche numeri TC.
Questa capacità può essere caratterizzata, per un specifico valore di contrasto, da due diversi parametri
Gli oggetti test relativi al primo parametro sono di solito composti da oggetti simili di varie dimensioni, ad esempio inserti circolari con diametro decrescente, e in genere sono riferiti a diversi valori di contrasto, come ad esempio la sezione dedicata del fantoccio CatPhan. (figura 3.2).
Gli oggetti test relativi alla valutazione della risoluzione a basso contrasto sono invece composti da inserti di forma varia (circolari o barre), costituiti da due materiali a basso contrasto tra loro e disposti a diverse frequenze spaziali, esattamente come lo sono quelli per la valutazione della risoluzione spaziale ad alto contrasto. In questo caso però il contrasto è unico e quello che varia è la frequenza spaziale dei dettagli. Un esempio è la sezione a basso contrasto del fantoccio multipurpose dell’AAPM, in genere definito come ATS Phantom (figura 3.1). Di fatto risulta consigliabile utilizzare la prima tipologia di misura.
Figura 3.1: schema e immagine TC della sezione del fantoccio del fantoccio AAPM – Nuclear Associates [44]
Figura 3.2: immagine TC della sezione del fantoccio Catphan per il basso contrasto
La rilevabilità a basso contrasto (low contrast detectability o LCD) è una valutazione importante di un sistema di immagine perché definisce la dimensione minima visibile di oggetti di basso contrasto ([2], [4], [14], [16] ).
Le informazioni fornite dal costruttore dovrebbero essere verificate in fase di accettazione dell’apparecchiatura. Le misure di LCD non devono necessariamente essere eseguite nelle prove di costanza poiché le componenti che influenzano il parametro cioè il rumore dell’immagine, la risoluzione spaziale ad alto contrasto e la dose al paziente sono controllate separatamente.
La difficoltà principale nella valutazione della risoluzione a basso contrasto è che richiede una valutazione soggettiva di dettagli di immagini da parte di un osservatore e quindi non fornisce un risultato rigorosamente quantitativo; tuttavia il parametro è un indice del prodotto finale del sistema e di come l’immagine viene percepita.
La rilevabilità a basso contrasto è comunemente definita con un singolo valore, che rappresenta il diametro del minimo oggetto rilevabile, per un determinato valore di contrasto e per un determinato valore di dose in ingresso al fantoccio. Vanno inoltre riportati, per completare la descrizione delle condizioni di acquisizione, lo spessore di strato e il filtro di ricostruzione.
Una descrizione più completa della rilevabilità di oggetti andrebbe definita con la curva dettaglio-contrasto, come riportato nella Fig.3.3.
Figura 3.3 : Curva contrasto-dettaglio [16]
Questa curva fornisce la risoluzione percepita per un ampio intervallo di contrasto. La forma della curva è però influenzata da una combinazione di rumore e di risoluzione spaziale, cioè dalla maggior parte dei parametri di acquisizione a questi connessi come i mAs, i kV, lo spessore di strato e gli algoritmi di ricostruzione.
Il contrasto percentuale è di solito definito come:
(3.5)
dove %C è il contrasto percentuale, TCoggetto è il numero TC dell’oggetto, TCfondo è il numero TC del materiale che costituisce il fondo, TCaria è il numero TC dell’aria.
Quando il materiale di fondo è l’acqua, l’equazione si semplifica:
(3.6)
3.5.2 Metodi di misura
Un oggetto test per la risoluzione a basso contrasto consiste di un numero di oggetti di diverse dimensioni che hanno uno specifico contrasto o diversi contrasti nominali. I diversi valori di contrasto si ottengono sia variando la composizione del materiale sia sfruttando gli effetti di volume parziale creati dall’oggetto che riempie in modo diverso il volume acquisito.
I valori di contrasto forniti per gli oggetti test commerciali sono nominali e, per una accurata caratterizzazione della risoluzione a basso contrasto, andrebbero misurati su ciascun tomografo e per tutti i diversi protocolli di acquisizione. È necessario però tenere in considerazione l’ampia variabilità dei valori di contrasto in funzione dello spettro della radiazione e della dipendenza dalla temperatura; per quest’ultima si riportano nel caso del ATS Phantom infatti inversioni di contrasto (da 6.9 HU a –1.7HU) tra i due materiali dell’oggetto test (acqua distillata inserita nei fori e il disco di silicone che costituisce il fantoccio) per variazioni di temperatura da 15°C a 35°C [14].
L’oggetto test è in genere posizionato all’isocentro e dopo aver acquisito il volume di interesse si valuta sull’immagine l’oggetto di minori dimensioni percepibile a parità di contrasto. Per eseguire il test in modo adeguato si devono acquisire un numero sufficiente di immagini, avere diversi osservatori e valutare l’immagine con un’opportuna illuminazione ambientale. Dovrebbe essere, pertanto, definito un adeguato protocollo per la visualizzazione delle immagini; questo può essere definito da un valore di finestra e da un n.TC medio oppure, alternativamente, può essere scelta dall’osservatore la miglior condizione di visualizzazione.
L’analisi del basso contrasto può essere anche condotta in modalità di acquisizione spirale, posto che l’oggetto test sia sufficientemente lungo per il volume di acquisizione impostato. Si sottolinea che costruttori tendono a non definire valori nominali di contrasto per acquisizioni spirali.
Le stesse considerazioni sulla lunghezza dell’oggetto test valgono anche nel caso di acquisizioni multistrato sia assiali che spirali.
3.5.3 Condizioni operative
I valori di riferimento forniti dai costruttori definiscono la rilevabilità a basso contrasto solo come dimensione minima rilevabile per una singola coppia di valore di contrasto e dose all’ingresso. I dati forniti non sono in genere accompagnati da indicazioni relative allo spessore di acquisizione e all’algoritmo di ricostruzione utilizzato in fase di misura. Per i tomografi a singolo strato viene in genere utilizzato lo spessore 10 mm e gli algoritmi più utilizzati nella routine; per una più corretta interpretazione delle misure eseguite in fase di accettazione queste informazioni dovrebbero essere richieste al costruttore.
Per verificare le specifiche del costruttore, in termini di LCD, è possibile effettuare correzioni anche se è consigliabile utilizzare esattamente le stesse modalità di acquisizione.
In alternativa alla valutazione visiva della LCD è possibile combinare numericamente o graficamente i valori di rumore, dose, spessore di strato e la risoluzione spaziale.
Ci sono relazioni teoriche che sono state definite da studi sui primi tomografi che spesso sono utilizzate a tale scopo [16]. Queste relazioni possono essere utilizzate [25] per correggere i dati di risoluzione a basso contrasto e per confrontare i risultati ottenuti in diverse condizioni di rumore, contrasto o risoluzione come mostrato nell’equazione successiva. La relazione tra rumore, dose e spessore di strato è ben nota dalla teoria; comunque la complessità dei tomografi più recenti ha mostrato che tali relazioni vanno trattate con cautela poiché possono essere ricavate empiricamente solo per alcuni algoritmi standard di ricostruzione.
Se è possibile è preferibile acquisire le immagini con i parametri corretti poiché la relazione è soggetta ad approssimazioni
(3.7)
Dove:
T = spessore di strato nominale o misurato (mm)
σ = deviazione standard normalizzata (%)
R = dimensione minima rilevabile (mm)
D = dose (mGy).
3.5.4 Dispositivo di prova
Per la descrizione dei dispositivi di prova si rimanda al capitolo relativo ai fantocci per la valutazione della qualità in TCMS. Si ricorda che la rilevabilità a basso contrasto dipende dalle dimensioni dell’oggetto test e dalla sua composizione e che i fantocci test più comuni utilizzati delle ditte costruttrici di tomografi per la determinazione dei valori di riferimento dell’LCD sono l’inserto a basso contrasto del Catphan o del Gammex, oppure l’inserto ATS che è una parte del fantoccio AAPM. Come visto in premessa in realtà il fantoccio AAPM serve a valutare la risoluzione a basso contrasto, per l’unico valore di contrasto dell’oggetto test, che come abbiamo visto può variare da misura a misura e da tomografo a seconda dello spettro del fascio (quindi tensione, filtrazione, etc) e della temperatura.
3.6 Artefatti
3.6.1 Definizione e discussione
Le immagini TC possono presentare artefatti, cioè delle discrepanze sistematiche tra i numeri TC dell’immagine ricostruita e i coefficienti di attenuazione reali dell’oggetto esaminato.
E’ possibile classificare gli artefatti in base alla loro origine [51].
Tralasciamo ulteriori osservazioni per gli artefatti dei primi 3 tipi, per i quali valgono le stesse osservazioni dei tomografi tradizionali, per concentrarci sui problemi tipici legati alle tecnologie spirale e multistrato.
3.6.1.1 Processi di interpolazione lungo l’asse z
La tecnica di acquisizione a spirale, che comporta un allargamento della SSP per i tomografi a singolo strato, e i processi di interpolazione che utilizzano modelli di ricostruzione lineari (180°LI o 360°LI), possono generare specifici artefatti di volume parziale. Questi artefatti sono particolarmente rilevanti in corrispondenza di dettagli che presentano una variazione accentuata lungo l’asse z, sia in termini di forma che di posizione, e per questo vengono “visti” dai rivelatori secondo angoli diversi lungo la traiettoria spirale. L’immagine della sezione di un cono acquisito con tecnica spirale ha la forma di una ellisse distorta che varia la sua orientazione (Fig. 3.4), mentre l’immagine della sezione di una struttura cilindrica inclinata rispetto al piano di scansione è costante in termini di forma ma presenta artefatti a banda che si irradiano all’intorno (Fig. 3.5)
Figura 3.4: immagini di un cono orientato lungo l’asse z acquisite in modalità spirale. [52]
Figura 3.5: immagini di un oggetto cilindrico inclinato lungo l’asse z acquisite in modalità spirale. [52]
La comparsa e la rilevanza di questi artefatti dipende dalla scelta del pitch e dal tipo di interpolazione impiegata [7]. Per ridurre questo tipo di artefatto occorre:
I processi di interpolazione delle TCMS producono una forma più complessa di distorsione delle immagini che dà luogo a un artefatto indicato con il termine di “mulino a vento”.
Figura 3.6: artefatti a mulino a vento [19]
Questa forma tipica è dovuta al fatto che i diversi canali di rivelazione intersecano il piano di ricostruzione dell’immagine durante la rotazione del tubo RX. Gli angoli formati dalle “pale” sono uguali alla differenza tra le posizioni angolari in corrispondenza delle quali file consecutive di rivelatori intersecano il piano dell’immagine. Indicando con pd il pitch riferito all’ampiezza di un singolo rivelatore [Eq. 1.2], gli angoli α risultano uguali a 360°/pd.
Figura 3.7: Immagine assiale di un oggetto sferico ottenuta con pd = 3 e algoritmo 180°LI. Gli angoli formati dalle tre linee continue corrispondono a circa 120° [53].
Pertanto, il numero di “pale” visibili è proporzionale al numero di canali che intersecano tale piano e aumenta quando:
E’ possibile limitare la rilevanza di questi artefatti utilizzando degli algoritmi di interpolazione del tipo z-filtering.
Figura 3.8: effetti dell’algoritmo di interpolazione sull’artefatto a “mulino a vento” [7]
3.6.1.2 Geometria del fascio radiante
Con l’aumento del numero degli strati, si è passati da una geometria fan beam (Fig. 3.9-a) a una geometria cone beam (Fig. 3.9-b).
Ne deriva che il piano formato da ciascun canale di rivelazione non è più perpendicolare all’asse del paziente, violando così un assunto di base della retro-ricostruzione 2D. L’errata registrazione dei dati (Figura 1.6) comporta la formazione di artefatti di volume parziale che risultano più evidenti su strutture che variano in modo accentuato lungo l’asse z e all’aumentare del pitch.
Per risolvere i problemi legati alla geometria conica, le case produttrici impiegano algoritmi di correzione cone beam.
Figura 3.11: effetti di un algoritmo di interpolazione standard e un algoritmo di correzione cone beam [54]
3.6.1.3 Elaborazioni tridimensionali
L’artefatto a “zebra” è tipico della tecnica spirale, è divenuto frequente con le TCMS ed è visibile nelle ricostruzioni MIP. Esso consiste di bande chiare e scure non parallele ai piani delle immagini ricostruite ed è originato dalla non uniforme distribuzione del rumore all’interno dell’immagine ricostruita, dovuta all’interazione tra gli algoritmi di interpolazione spirale e gli algoritmi di retro-proiezione del fascio.
Figura 3.12: artefatto a “zebra” in un’immagine MIP [51]
Tale disuniformità è correlata con le posizioni angolari del tubo che definiscono il set di dati utilizzati per ricostruire l’immagine. Il rumore dell’immagine segue pertanto un andamento ciclico, passando da un valore massimo in prossimità delle posizioni angolari vicine agli estremi dell’intervallo di ricostruzione a un valore minimo in corrispondenza della parte centrale del set di dati. Tale fenomeno si verifica una sola volta per rotazione su un tomografo a strato singolo che impiega un algoritmo di ricostruzione lineare 180°LI, ma nei tomografi MS aumenta proporzionalmente con il numero di canali impiegati.
In fase di elaborazione dell’immagine MIP, alle regioni caratterizzate da valori più elevati di rumore verrà assegnato un valore MIP più elevato, perché è più alta la probabilità di avere numeri CT molto al di sopra della media. L’andamento ciclico del rumore all’interno delle immagini ricostruite si traduce in una rappresentazione periodica di bande alternate chiare e scure all’interno dell’immagine MIP che non sono parallele al piano di ricostruzione delle immagini, in quanto ciascuna immagine presenta una zona ad alto rumore (che contribuisce alla banda chiara) e una a basso rumore (banda scura).
L’artefatto Venetian blind è tipico della tecnica spirale multistrato ed è visibile nelle ricostruzioni MIP. Consiste in bande chiare e scure parallele all’asse orizzontale dell’immagine MIP.
Figura 3.13: artefatto Venetian blind in un’immagine MIP; l’artefatto è più pronunciato nella regione pelvica, dove il fascio è più attenuato [55].
L’artefatto è prodotto dall’intensità del rumore all’interno di ogni singola immagine ricostruita e dalla variazione dello stesso rumore da un’immagine all’altra. Tale variazione dipende dal fatto che il rumore di una proiezione è funzione del corrispondente angolo di proiezione.
Le condizioni che favoriscono l’artefatto, per le quali è maggiore l’entità della variazione del rumore in ciascun intervallo angolare di 2π, sono:
Figura 3.14: artefatto Venetian blind a diversi valori di pitch: 0.5625:1, 0.9375:1, 1.375:1 e 1.75:1 (dall’alto verso il basso) [55].
E’ possibile ridurre la variazione del rumore:
3.6.1.4 Inclinazione del gantry
L’inclinazione del gantry può influire sulla prestazione degli algoritmi di ricostruzione spirale nei tomografi TCMS, producendo gravi artefatti nell’immagine, quali la distorsione o la discontinuità di dettagli anatomici.
A causa dell’inclinazione del gantry, infatti, l’isocentro di ricostruzione dei canali più esterni non coincide con l’isocentro del gantry e si possono avere tanti isocentri di ricostruzione quanti sono i canali utilizzati per ricostruire l’immagine. Si spiega così il motivo per cui alcune delle strutture ricostruite risultano spostate e sovrapposte, mentre altre appaiono scarsamente definite.
Per ridurre o eliminare gli effetti del disallineamento degli isocentri sono stati sviluppati sistemi di compensazione mediante il riallineamento delle proiezioni oppure mediante correzioni in fase di retro-proiezione.
3.6.1.5 Diversa risposta dei singoli canali di acquisizione
L’utilizzo dei tomografi multistrato in modalità assiale comporta che le immagini di regioni anatomiche contigue siano acquisite da canali di acquisizione diversi. Un difetto di funzionamento, un’errata calibrazione o qualsiasi altro inconveniente a carico di un solo canale può dar luogo a un artefatto visibile solo sulle immagini acquisite con quel singolo canale, simulando la presenza di lesioni patologiche.
Figura 3.15: Esame assiale dell’encefalo con tomografo a quattro strati – Area iper-densa presente solo su una immagine ogni quattro [56].
3.6.2 Metodi di misura
Come già osservato nel capitolo relativo ai fantocci, solo recentemente troviamo in commercio oggetti test specifici che permettano di quantificare l’entità e le caratteristiche dell’artefatto. Inoltre è difficile definire dei veri e propri metodi di misura: in prima analisi è possibile effettuare valutazioni visive che forniscano per confronto delle informazioni sull’entità e le caratteristiche dell’artefatto. Ad esempio è utile confrontare come variano gli artefatti al variare della configurazione di un tomografo MSTC o del pitch.
Con l’introduzione degli algoritmi di ricostruzione Cone Beam, l’effetto di questi artefatti viene ridotto più o meno efficacemente a secondo del tipo di algoritmo. Si confronti ad esempio la figura 3.16 con la figura 3.17: nella prima sono evidenti gli artefatti da Cone Beam, nella seconda si nota che con l’algoritmo AMPR (di tipo Cone Beam) viene migliorata la qualità dell’immagine [20].
Uno dei principali obiettivi delle ditte costruttrici di tomografi è orientato all’implementare tecniche di ricostruzione Cone Beam sempre più efficaci e veloci e per questo sono allo studio dei metodi che consentano di analizzare numericamente il beneficio dei diversi algoritmi [21].
Figura 3.16 MPR del fantoccio torace senza algoritmi di correzione Cone Beam [20]
16 rows pitch 1.0 16 rows pitch 1.5
Figura 3.17: MPR del fantoccio torace con algoritmo di ricostruzione AMPR [20]
Nella figura 3.18 è riportato un esempio relativo all’utilizzo del fantoccio tipo Clock phantom citato nel capitolo degli artefatti [7].
Figura 3.18 – Immagini del fantoccio Clock Phantom QRM con artefatti di tipo Cone Beam [7]
4 CARATTERISTICHE DELLO STRATO
Lo strato può essere definito in termini di strato irradiato e di spessore dello strato.
Lo spessore dello strato è un parametro di fondamentale importanza per determinare la risoluzione dell’immagine lungo l’asse z mentre lo spessore irradiato, o ampiezza del profilo di dose, è una misura della collimazione “pre paziente” del fascio radiante lungo l’asse z.
Sia nei tomografi a singolo strato che in quelli multistrato, si ha una prima collimazione del fascio di raggi X lungo l’asse z (collimazione “pre paziente”); dopo l’irradiazione del paziente, l’ampiezza del fascio può essere ulteriormente modificata dai collimatori “post paziente”. Lo scopo di questa seconda collimazione è quello di ridurre la radiazione diffusa sui collimatori e di ottenere uno strato più sottile di quello che sia possibile ottenere impiegando semplicemente una collimazione “pre paziente”. Nei tomografi multistrato la post collimazione può essere impiegata anche per escludere alcuni elementi di rilevazione ed ottenere quindi degli strati più sottili delle effettive dimensioni dei rivelatori (narrow collimation). Tuttavia nei sistemi multistrato oggi in commercio la post-collimazione non è quasi mai presente.
In un sistema ideale, lo spessore dello strato e lo spessore irradiato coincidono; in realtà lo spessore irradiato è sempre maggiore dello spessore dello strato. Questo fenomeno si verifica in maniera più accentuata nei tomografi multistrato dove lo spessore irradiato è più ampio per assicurare che tutti gli elementi di rivelazione impiegati per la formazione dell’immagine siano irradiati uniformemente.
4.1 Spessore irradiato
Per verificare la collimazione del fascio di radiazione in direzione z si misura lo spessore irradiato. Le misure vengono solitamente eseguite in modalità assiale; non è necessario ripeterle in modalità spirale perché la collimazione non dipende dal tipo di acquisizione.
4.1.1 Metodi di misura
Lo spessore irradiato è definito in termini di larghezza a metà altezza (FWHM) o a un decimo dell’altezza (FWTM) del profilo di dose che può essere misurato utilizzando i dosimetri a termoluminescenza o pellicole a bassa sensibilità; lo spessore irradiato viene solitamente misurato all’isocentro, perché le ditte produttrici forniscono le specifiche dello spessore dello strato nominale in questa posizione.
I TLD possono essere utilizzati solo per la valutazione di spessori superiori a 2 mm; per spessori irradiati più sottili, le dimensioni dei rivelatori limitano l’accuratezza dei profili. Per spessori sottili è necessario utilizzare le pellicole radiografiche.
La pellicola viene posizionata perpendicolarmente al piano di scansione in corrispondenza dell’isocentro; per limitare la radiazione diffusa dal tavolo, è opportuno collocarla su un supporto di polistirolo. Dopo aver sviluppato la pellicola, si ricava la FWHM del profilo di densità ottica, ottenuto digitalizzando il film. Per avere un’accuratezza migliore si può convertire il profilo di densità ottiche in un profilo di dose utilizzando una curva di calibrazione dose-densità ottica. Si suggerisce di utilizzare film per la verifica di radioterapia oppure film dentali o industriali.
Un nuovo tipo di pellicola utilizzabile è la pellicola “Gafchromic ® XR-CT (ISP – 1361 Alps Road, Wayne, NJ 07470) [39]. Si tratta di una pellicola autosviluppante di sensibilità idonea per misure di profili di dose in TC (intervallo di esposizione da 0.5 a 100 mGy circa), oltre che a misure di dose. La larghezza del profilo può essere misurata direttamente, oppure digitalizzata con scanner ottico riflessivo da banco (fig. 4.1).
Una volta ottenuto il profilo, oltre a misurare la FWHM e la FWTM, si può analizzare la sua forma per vedere quanto si avvicina a un profilo rettangolare. Questa analisi può dare informazioni sulla collimazione, sulla geometria dei rivelatori e sulla macchia focale.
Figura 4.1: schema ed esempio di pellicola gafchromic impressionata [39]
4.1.2 Considerazioni per tomografi multistrato
Nei tomografi multistrato si può misurare lo spessore irradiato con gli stessi metodi descritti per i tomografi a singolo strato. In generale si osserva che lo spessore irradiato è maggiore della somma degli spessori degli strati della configurazione utilizzata per ottenere un certo spessore totale; questo si verifica perché è necessario avere un’irradiazione uniforme di tutti i rivelatori utilizzati, e quindi la penombra del fascio si estende oltre gli elementi di rivelazione più esterni che vengono utilizzati per creare lo strato.
4.1.3 Condizioni operative
Le misure dello spessore irradiato devono essere eseguite per ogni collimazione possibile sia per TC singolo strato che multistrato.
Il profilo dipende dalle dimensioni della macchia focale, in particolare per le collimazioni sottili, e non dipende dal FOV.
4.2 Spessore dello strato
Lo spessore dello strato definisce l’effettiva sezione tomografica che tiene conto sia della collimazione del fascio in uscita dal tubo radiogeno, sia, molto spesso, di una post-collimazione del sistema di rivelatori. Nei sistemi spirali sia a singolo che multistrato inoltre la forma del profilo dipende fortemente dalle tecniche di ricostruzione lungo z. Lo spessore dello strato ricostruito è generalmente espresso in termini di FWHM e FWTM del profilo di sensibilità lungo l’asse z (SSP).
Per misurare lo spessore dello strato in modalità assiale si utilizza un fantoccio pieno di acqua o di materiale omogeneo in cui è inserito un oggetto test sottile e ad alto contrasto, come un foglio sottile di alluminio, inclinato rispetto al piano di scansione (rampa). È possibile anche utilizzare due rampe che si incrociano a formare una “X” e che siano posizionate simmetricamente rispetto all’asse z in modo tale da riuscire a correggere eventuali disallineamenti del fantoccio mediando le misure ottenute sulle due rampe.
Figura 4.2: fantoccio utilizzato per misurare lo spessore dello strato [16]
L’immagine delle rampe viene generalmente acquisita nel piano in cui si incrociano; il contributo della rampa di alluminio presente nell’immagine dipende dello spessore dello strato e dall’angolo che la rampa forma con il piano di scansione.
Mettendo in grafico i valori dei numeri TC di entrambe le rampe in funzione della distanza si calcolano dai profili i valori di FWHM. Lo spessore dello strato si ottiene quindi dalla seguente equazione:
(4.1) s = d x tg(θ )
dove s è lo spessore dello strato (FWHM) in mm, d è la FWHM misurata sul profilo, θ l’angolo di inclinazione della rampa di alluminio rispetto all’asse x.
Se si utilizzano oggetti test con due rampe di alluminio, si può calcolare lo spessore dello strato a partire dal valore medio degli spessori ottenuti sulle due rampe. I profili dei numeri CT saranno identici se le rampe sono allineate e centrate correttamente rispetto al piano tomografico. In presenza di disallineamenti tra l’asse z del fantoccio e l’asse del tomografo i due profili saranno diversi, ma mediando i risultati si possono elidere le differenze.
I fantocci disponibili in commercio hanno inserti che formano con il piano di scansione angoli di 25°, 30° o 45°. Con un angolo di 45° il fattore correttivo è pari a 1 e quindi si può avere una misura di spessore di strato direttamente dal profilo dei numeri TC.
4.2.2 Metodi di misura: modalità spirale
Il metodo classico della rampa inclinata non è adatto ad analizzare lo spessore dello strato ricostruito per scansioni spirale, a causa degli artefatti da interpolazione che nascono dalla presenza di oggetti ad alto contrasto posti con una certa angolazione rispetto al piano dell’immagine. Per valutare lo spessore dello strato in modalità spirale è necessario ricorrere a un metodo alternativo, utilizzando fantocci dedicati. Tali fantocci contengono una sferetta (con diametro submillimetrico) o un foglio sottile di materiale ad alto contrasto (ad esempio tungsteno) [16, 22].
Figura 4.3 fantoccio per la misura dello spessore dello strato in modalità spirale [16]
I fantocci con un dischetto di materiale ad alta densità sono meno pratici di quelli con la sferetta, perché hanno problemi di allineamento; tuttavia, nel caso di fantocci contenenti la sferetta si hanno problemi legati al rapporto segnale-rumore, perché per ricavare il numero TC si utilizzano ROI molto piccole (1-2 pixel).
Per misurare lo spessore dello strato in modalità spirale si effettua una acquisizione centrata sull’inserto e si ricostruiscono le immagini a intervalli che non devono essere superiori ad 1/10 dello spessore dello strato; per ogni strato si registra poi il valore massimo (o il valore medio) del numero TC di una ROI centrata sull’inserto. In genere se l’inserto è una sfera si preferisce prendere il massimo, se l’inserto è un disco si prende la media. Tale ROI deve essere grande a sufficienza per minimizzare le fluttuazioni statistiche dei numeri TC ma piccola a sufficienza per minimizzare ogni errore dovuto a un eventuale disallineamento del disco.
La curva SSP (slice sensitivity profile, che rappresenta il profilo di sensibilità in direzione z) si ottiene mettendo in grafico i valori dei numeri TC in funzione della distanza; la FWHM della curva così ricavata è una misura dello spessore dello strato in modalità spirale. Tuttavia la FWHM non è un descrittore completo della curva di sensibilità lungo l’asse z, dal momento che la forma del profilo si allarga e cambia di forma in immagini acquisite in spirale rispetto alle immagini acquisite in assiale ed inoltre tale forma dipende dal pitch e dagli algoritmi di interpolazione. Possono quindi essere introdotti ulteriori descrittori: FWTM e FWTA (full width at tenth area).
Si può prevedere lo spessore dello strato ricostruito in una acquisizione spirale per diversi valori di pitch e per diversi algoritmi di interpolazione (tabella 4.1). Questi rapporti possono essere riportati anche ad altri spessori di strato.
Spessore nominale (mm) | Spessore misurato (mm) | ||||
Assiale | Spirale pitch 1 | Spirale pitch 2 | |||
360 LI | 180LI | 360LI | 180LI | ||
5 | 5 | 6.3 | 5 | 10.8 | 6.5 |
Tabella4.1: spessori dello strato in modalità spirale [16]
Il metodo della sferetta o del dischetto può essere utilizzato anche per scansioni assiali, incrementando la posizione dell’oggetto test a piccoli intervalli lungo l’asse z ed acquisendo in corrispondenza di ogni posizione per ottenere una serie di immagini. Ovviamente questo metodo è influenzato dall’accuratezza del movimento del lettino.
4.2.3 Metodi di misura: tomografi multistrato
I metodi descritti sopra possono essere utilizzati anche per valutare lo spessore dello strato di tomografi multistrato.
Per acquisizioni in assiale è opportuno valutare lo spessore di ogni singolo strato e confrontare sia i valori ottenuti su diversi strati a parità di collimazione che i valori ottenuti per diverse configurazioni di rivelatori, a parità di spessore nominale, per verificare che ci sia consistenza tra di essi.
Le rampe inclinate contenute nei fantocci devono essere lunghe a sufficienza da comprendere tutte le immagini acquisite simultaneamente in assiale; nel caso in cui l’oggetto test non sia lungo a sufficienza, si può analizzare ogni immagine separatamente spostando la posizione di scansione per assicurare che le immagini ottenute da ogni gruppo di rivelatori coincida con la parte centrale dell’oggetto test.
Lo spessore dello strato per acquisizioni assiali dipende dalle collimazioni pre e post paziente; per acquisizioni spirale dipende anche dal pitch e dall’algoritmo di interpolazione.
Per acquisizioni in spirale, i tomografi multistrato utilizzano algoritmi diversi da quelli impiegati nei tomografi a singolo strato in modo tale da fare un uso ottimale dei dati disponibili. Utilizzando quindi degli algoritmi di z filtering (vedi paragrafo 1.2) con diverse funzioni peso si possono ottenere immagini il cui spessore di strato è invariante con il pitch.
Il profilo di sensibilità in direzione z è dipendente dalle macchia focale utilizzata, in particolare per le collimazioni sottili. Alcuni tomografi hanno due macchie focali che sono selezionate automaticamente in dipendenza dai parametri di scansione. Per esempio, la macchia focale piccola può essere selezionata solo con spessori sottili, bassa corrente nel tubo ed algoritmi ad alta risoluzione.
Il profilo di sensibilità è indipendente dal kernel di convoluzione utilizzato nella ricostruzione dell’immagine assiale. Tuttavia, se vengono utilizzati algoritmi ad alta risoluzione o algoritmi molto smoothing si possono avere delle differenze; è consigliabile, quindi, acquisire i profili utilizzando algoritmi standard.
Infine, il FOV di scansione non influenza lo spessore dello strato mentre il FOV di ricostruzione influisce sull’accuratezza delle misure di spessore eseguite con fantocci contenenti le rampe incrociate perché tale accuratezza dipende dalle dimensioni del pixel: è quindi consigliabile utilizzare un FOV piccolo per avere una minore dimensione del pixel.
Come già spiegato nella sezione relativa agli oggetti test, la misura di spessori sottili è critica, e questo problema si manifesta correntemente nei sistemi a 16 o 64 strati dove le dimensioni del rivelatore consentono di ricostruire spessori da 0.5 o 0.6. In questo caso occorre avere rampe con angoli di inclinazione piccoli (es 5°) e di spessore piccolo (es: 180 µm).
4.3 Efficienza geometrica
L’efficienza geometrica di un fascio di raggi X indica la percentuale del fascio di radiazione che viene utilizzata nel processo di formazione dell’immagine; l’efficienza geometrica può essere distinta in due componenti [8]:
4.3.1 Efficienza geometrica lungo l’asse z
Nella norma IEC 60601-2-44 (Ed. 1, 1999) [40] l’efficienza geometrica è definita come la FWHM del profilo di sensibilità (spessore dello strato) espressa come percentuale della FWHM del profilo di dose:
(4.2)
Nella norma IEC 60601-2-44 (Ed. 2, 2003) [41] è stata introdotta una nuova definizione, secondo cui l’efficienza geometrica è l’integrale del profilo della dose nella direzione z, integrato sul range sotteso dagli elementi del rivelatore utilizzati durante l’acquisizione, espressa come percentuale dell’integrale di tutto il profilo della dose nella direzione z (Figura 4.4):
(4.3)
In entrambi i casi la norma raccomanda che il valore dell’efficienza sia visualizzato sulla consolle qualora sia inferiore al 70%. Per un impiego ottimale della dose l’efficienza geometrica dovrebbe essere prossima al 100%.
Secondo la vecchia definizione quindi l’efficienza geometrica è il rapporto tra lo spessore dello strato e lo spessore irradiato; secondo la nuova definizione è il rapporto tra l’integrale del profilo della dose su un range pari allo spessore nominale dello strato e l’integrale dell’intero profilo della dose.
Per misurare l’efficienza geometrica secondo la vecchia definizione è necessario disporre dei valori dello spessore di strato e della FWHM del profilo della dose lungo l’asse z.
I limiti connessi alla definizione del 1999 sono legati alle differenti condizioni di misura (misura in aria per lo spessore irradiato e in fantoccio per lo spessore dello strato) e, nel caso di TCMS, alla necessità di eseguire molteplici misure, poiché ogni spessore di strato si può ottenere mediante diverse configurazioni. Inoltre, nel caso di strati sottili (< 1 mm), i valori dello spessore dello strato ottenuti con il metodo della rampa inclinata inclusa nei fantocci attualmente disponibili non sono accurati, e portano quindi a un’indeterminazione sul valore dell’efficienza geometrica stessa.
Figura 4.4: le due definizioni di efficienza geometrica [23]
Anche la nuova definizione non è comunque esente da problemi legati al fatto che non è definita la posizione del profilo della dose rispetto ai rivelatori. Se si vuole calcolare l’efficienza geometrica secondo la definizione del 2003, sono, quindi, possibili due diversi approcci: o centrare il range di integrazione sul centro del profilo della dose a metà della FWHM, oppure scegliere la posizione del range che dà la massima efficienza geometrica. I valori di efficienza determinati mediante i due approcci hanno una differenza massima pari allo 0.04% nel caso di CT a singolo strato e di 0.6% per TCMS, e una differenza media pari a 0.1% [23] e pertanto sono sostanzialmente equivalenti.
Nella figura 4.5 sono riportati i risultati di misure di efficienza su alcuni tomografi di nuova generazione: si nota che l’efficienza lungo l’asse z cresce all’aumentare della collimazione, arrivando comunque a un valore di saturazione che non è ulteriormente migliorabile.
Nei sistemi TCMS si verifica infatti il fenomeno dell’overbeaming, cioè si impiega un fascio di radiazione più largo di quello che sarebbe richiesto in sistemi a singolo strato, per assicurare che tutti i rivelatori che vengono utilizzati per la formazione dell’immagine siano irradiati uniformemente. Questa parte di fascio “extra” è generalmente fissata ed è in proporzione maggiore per spessori minori; ciò giustifica la caduta dell’efficienza alle basse collimazioni.
Nella figura 4.5 si mostra che le misure eseguite con le due definizioni di efficienza geometrica sopra descritte portano a risultati paragonabili tra loro con differenze contenute entro il 2% tranne che per strati sottili dove la definizione del 1999 tende a sovrastimare i valori.
Figura 4.5: efficienza geometrica lungo l’asse z
4.3.2 Efficienza geometrica del sistema di rivelazione
L’efficienza geometrica del sistema di rivelazione è definita come il rapporto tra l’area attiva e l’area totale del sistema di rivelazione.
L’area totale di rivelazione è costituita da materiale di rivelazione e da setti tra gli elementi di rivelazione, sia nel piano di scansione (piano x-y) che lungo l’asse z [8].
Figura 4.6: matrici di rivelatori per tomografi multistrato a 8 e 16 strati: Il tomografo a 16 strati ha approssimativamente il doppio del numero di setti lungo l’asse z [8]
In generale, man mano che aumenta il numero di strati acquisiti simultaneamente, la dimensione degli elementi di rivelazione lungo l’asse z diminuisce; ciò comporta un aumento del numero di setti e quindi una diminuzione dell’efficienza geometrica del sistema di rivelazione. Tale effetto è mostrato nella tabella 2 per i tomografi Philips Mx8000: in questo esempio la diminuzione dell’efficienza geometrica passando da un sistema a 2 strati a uno a 16 strati è del 5%. Questo valore naturalmente dipende dalla configurazione del sistema di rivelazione; si ha comunque una tendenza verso valori di efficienza più bassi man mano che aumenta il numero di rivelatori per unità di lunghezza.
Numero di strati | Numero di banchi di rivelatori | Copertura lungo l’asse z (mm) | Efficienza del sistema di rivelazione (%) |
2 | 2 | 20 | 80 |
4 | 8 | 20 | 78 |
16 | 24 | 24 | 75 |
Tabella 4.2: efficienza geometrica del sistema di rivelazione per tomografi Philips
Mx8000 [8].
5 INDICI DI DOSE
La scelta degli indici di dose e dei metodi di misura dipende dallo scopo che ci si prefigge; in fase di accettazione dell’apparecchiatura tomografica, generalmente, è necessario effettuare le misure in fantoccio standard di PMMA per confrontare i dati con le specifiche delle Ditte costruttrici. Per le prove di costanza può essere sufficiente effettuare solo la misura in aria dell’output del tubo.
Le misure in fantoccio standard di PMMA dovrebbero essere utilizzate per confrontare diversi tomografi e protocolli diversi o per la verifica dei livelli diagnostici di riferimento (LDR).
I parametri dosimetrici possono essere misurati a partire da una scansione singola assiale da cui è possibile ricavare l’indice di dose della tomografia computerizzata (CTDI)
5.1 Indice di Dose per Tomografia Computerizzata (CTDI)
5.1.1 Definizioni
Il CTDI (Computed Tomography Dose Index) è definito nel seguente modo:
(5.1)
dove:
z1,z2 = limiti di integrazione lungo l’asse z
D (z) = profilo di dose lungo una singola scansione assiale
n = numero di strati acquisiti simultaneamente (n=1 per tomografi a singolo
strato, n=4 per un tomografi a 4 strati, etc.)
T = lo spessore nominale dello strato o l’ampiezza del gruppo di rivelatori nel
caso di TC multistrato (per esempio 5 mm per una acquisizione 4 x 5 mm)
Il CTDI può facilmente essere misurato usando una camera a ionizzazione a stilo lunga 10 cm. In tal caso la formula ha dei precisi limiti di integrazione in quanto z1 e z2 sono uguali a ± 5 cm coprendo una lunghezza totale di 10 cm e abitualmente viene scritto come CTDI100 dove il pedice indica l’estensione su cui è stata effettuata l’integrazione.
5.1.2 Metodi di misura
La camera a ionizzazione deve essere allineata con l’asse z del tomografo e irradiata con una scansione assiale impostando un singolo strato al centro della lunghezza della camera. La camera ha una risposta lineare lungo la sua lunghezza e generalmente viene calibrata con un campo uniforme che la copre interamente. Il valore ottenuto con una singola scansione è il valore medio dell’esposizione o della dose lungo la camera . Viene quindi applicato il fattore di calibrazione della camera e, se necessario, il fattore per la conversione in dose. Per una maggior accuratezza la misura deve essere moltiplicata per il fattore di correzione per la temperatura e la pressione. L’integrale del profilo della dose è calcolato moltiplicando la dose misurata per la lunghezza della camera. Infine questo ultimo valore diviso per lo spessore nominale dello strato è il CTDI100.
(5.2) mGy
dove:
R = Kerma in aria misurato (mGy) corretto per il fattore di correzione per la
temperatura e la pressione
cfE = fattore di calibrazione per la camera a ionizzazione a una appropriata energia
(55 keV per misure in aria, 70 keV per misure in fantoccio)
L = lunghezza della camera a ionizzazione (100 mm)
n = numero di strati acquisiti simultaneamente
T = lo spessore nominale dello strato o l’ampiezza del gruppo di rivelatori nel caso di TC multistrato
Il CTDI100 è misurato in mGy per un determinato valore di mAs oppure può essere normalizzato, nCTDI100, e misurato in mGy/mAs.
Figura 5.1 Misura del CTDI [16]
Misure di dose in aria
Per una misura semplice dell’output del tubo si misura il CTDIaria con la camera a ionizzazione allineata lungo l’asse del tomografo all’isocentro.
Una variazione del CTDI può essere dovuta a una variazione della corrente nel tubo, della tensione o dell’ampiezza della collimazione del fascio. Anche la dimensione della macchia focale, la variazione di energia e dell’emissione del fascio dovuto alla differente filtrazione possono causare una variazione del CTDI. Se tale misura viene eseguita per monitorare l’output del tubo, allora bisogna misurare come riferimento anche il profilo della dose della singola sezione. A tal proposito è possibile usare i TLD oppure le pellicole radiografiche, o ancora le pellicola Gafchromic .
Per il test di costanza, se non si ha a disposizione una camera a ionizzazione dedicata, l’output può essere misurato con un’altra camera con geometria regolare e risposta sufficientemente uniforme.
Fantocci
Per le caratteristiche dei fantocci si rimanda alla sezione specifica (par.2.2)
Distribuzione di dose all’interno del fantoccio
La distribuzione di dose alla periferia del fantoccio non è generalmente uniforme a causa di un possibile overscan introdotto anche in modalità assiale per ridurre gli artefatti da movimento. Sono possibili anche effetti dovuti alla salita della tensione al tubo all’inizio della scansione, o una riduzione della dose nelle posizioni più basse a causa dell’attenuazione del lettino. Dalle misurazioni effettuate nelle posizioni previste dal fantoccio (ore 3, 6, 9 e 12 ) è possibile trovare il punto in cui la dose è massima e stabilire una media rappresentativa. Talvolta tuttavia la posizione in cui la dose assume il valore massimo può variare nelle scansioni successive e pertanto è difficile valutare la non uniformità di misura all’interno del fantoccio. La posizione iniziale della scansione può essere scelta e fissata generalmente solo in modalità service. In modalità di scansione clinica, per esempio, l’irraggiamento può iniziare nella stessa posizione angolare ogni volta, in una o due delle quattro posizioni, oppure il tubo può iniziare a irraggiare in un punto arbitrario. In queste condizioni dovrebbe essere effettuata una sequenza di misurazioni in una posizione periferica del fantoccio per determinare il range di valori ottenuti.
Durante l’installazione dell’apparecchiatura è necessario determinare la posizione di ogni eventuale sovraesposizione al fine di stabilire se è possibile evitare organi sensibili, come ad esempio gli occhi, quando si effettua una scansione in modalità assiale.
I valori di CTDI100 misurati in posizioni periferiche del fantoccio della testa sono spesso simili ai valori misurati al centro del fantoccio. Per il fantoccio “corpo”, tuttavia, i valori alla periferia sono generalmente circa il doppio dei valori misurati al centro del fantoccio. Il rapporto esatto dipende dall’energia efficace del fascio a raggi X, dalla forma del fascio e dalla filtrazione.
5.1.3 CTDI pesato (CTDIw)
I valori ottenuti al centro del fantoccio possono essere combinati con i valori alla periferia in modo tale da ottenere un valor medio pesato.
(5.3)
dove CTDI100,centro e CTDI100,periferia sono misurati al centro e alla periferia del fantoccio rispettivamente. Il valore alla periferia è una media di almeno quattro misure intorno al fantoccio.
Il CTDIw in fantoccio è definito nel documento della Comunità Europea “Quality Criteria and Reference Doses in CT” [24] ; tale indice è espresso in termini di dose assorbita in aria.
Gli standard di sicurezza raccomandano che il CTDIw sia indicato sulla consolle del tomografo per dare all’operatore un’indicazione, seppure approssimata, della dose al paziente.
Il CTDIw, così definito, non prevede nessuna correzione per il valore del pitch utilizzato nella scansione spirale; nella recente edizione dell’IEC sugli standard di sicurezza in TC [17] si utilizza un nuovo indice (CTDIvol) cioè il CTDIw corretto per il pitch (vedi par.5.1.4). Attualmente coesistono sulle apparecchiature in commercio le due grandezze CTDIw e CTDIvol, e ciò può essere potenzialmente fuorviante. E’ quindi estremamente importante che l’esperto in fisica medica esegua dei test che verifichino l’accuratezza degli indici di dose visualizzati sulla consolle dell’apparecchiatura tomografica.
5.1.4 CTDIvol (CTDIW mediato lungo asse z)
Il CTDI è un valore calcolato da misure effettuate utilizzando una singola scansione. Per strati contigui o per pitch uguale a uno, questo rappresenta direttamente la dose media lungo la lunghezza esaminata. Tuttavia, per strati non contigui o per pitch diversi da uno, deve essere applicato un fattore di correzione lungo l’asse z. La dose media nel piano della scansione è data dal CTDIw che combina le misure effettuate al centro e alla periferia del fantoccio. Quando viene applicato il fattore di correzione lungo l’asse z, il valore risultante rappresenta la dose media nel volume esaminato. Questo CTDIw corretto, può essere indicato come CTDIvol, che indica una dose mediata sul volume.
(5.4) CTDIvol = CTDIw × PF (modalità assiale)
(5.5) CTDIvol = CTDIw/pitch (modalità spirale)
PF è il packing factor che mette in relazione il movimento del tavolo con lo spessore dello strato in modalità assiale. In modalità spirale la relazione equivalente è data dall’inverso del pitch. PF e pitch sono così definiti:
(5.6) PF = PF =
Dove:
n = numero di strati acquisiti simultaneamente
T = spessore nominale dello strato o estensione del gruppo di rivelatori nel caso di TC multistrato
CI = distanza percorsa dal lettino per ogni rotazione del tubo
Il CTDIvol è equivalente al MSAD descritto nel prossimo paragrafo.
5.2 MSAD (Multiple scan average dose)
5.2.1 Definizione e discussione
La dose media lungo l’asse z, nello strato centrale di una serie di N strati, quando si è impostato un incremento costante I tra strati successivi, è nota come MSAD.
La MSAD è misurata al centro di una serie di scansioni sequenziali con un dato incremento del lettino, di solito uguale all’ampiezza nominale irradiata specificata dal costruttore. Dopo un numero di scansioni consecutive la dose media al centro delle serie raggiunge il valore massimo. Questo perché la dose nella regione centrale della scansione subisce anche il contributo delle “code” delle scansioni confinanti. La definizione è data dalla seguente equazione:
(5.7) MSAD =
Dove CI è l’incremento del lettino, D(z) è il profilo della dose risultante dall’intera serie di scansioni e l’origine dell’asse z è al centro della serie.
Benché la MSAD sia definita per scansioni assiali, può essere utilizzata anche nel caso di scansioni in modalità spirale e CI diventa il movimento del lettino per ogni rotazione del tubo. E’ da tener presente tuttavia che tale indice dosimetrico risulta ormai essere sostanzialmente superato e le valutazioni di dose vengono riportate perlopiù in termini di CTDI.
Figura 5.2 – Relazione tra CTDI e MSAD [16]
5.2.2 Relazione tra CTDI e MSAD
La MSAD risulta essere uguale al CTDI nel caso in cui l’incremento del lettino sia uguale allo spessore nominale dello strato irradiato e la lunghezza della scansione coincida con i limiti di integrazione del CTDI; ciò è evidenziato nella figura 5.2. La dose media al centro della serie di strati (MSAD) è composta dalla dose media della fetta centrale (ampiezza a metà altezza del profilo della dose) più il contributo di dose dovuto alle code degli strati adiacenti. L’integrale del profilo della dose del singolo strato include anche le code del profilo della dose e questo viene quindi mediato sullo spessore nominale dello strato per il calcolo del CTDI.
Nelle situazioni in cui il movimento del lettino non è lo stesso dello spessore nominale dello strato irradiato, la MSAD è uguale al CTDIvol.
5.3 Modalità spirale
Il CTDI è una misura definita per scansioni effettuate in modalità assiale pertanto non può essere strettamente applicata alla scansioni in spirale. Tuttavia è possibile, tramite il confronto tra misura in assiale e misura in spirale, ricavare un fattore correttivo per passare dal CTDIassiale al “CTDIspirale”.
Fattore di correzione per singola rotazione
La determinazione del fattore di correzione permette di stabilire l’entità di extra irraggiamento (overscan) dovuto a una scansione spirale; il fattore correttivo può, inoltre, essere utilizzato per il calcolo accurato del Prodotto Dose per Lunghezza, DLP (Dose Length Product) per l’irraggiamento in modalità spirale. Per calcolare il fattore di correzione le valutazioni dosimetriche devono essere eseguite su due scansioni dell’intera lunghezza della camera a ionizzazione: una scansione assiale a strati contigui e una spirale con pitch unitario.
Il rapporto tra le due letture sarà equivalente al rapporto tra modalità assiale e spirale per una rotazione del tubo.
Figura 5.3 Confronto tra misure di dose in spirale e assiale [16]
5.3.1 TC multistrato
La definizione del CTDI rimane valida anche nel caso di TC multistrato, dove il parametro n (Eq.5.1) rappresenta il numero di strati irradiati simultaneamente.
Il fattore di correzione per la scansione spirale può essere ottenuto come descritto per la TC a singolo strato. Tuttavia in alcune TC multistrato non è sempre possibile lavorare a pitch 1. Sarà quindi necessario effettuare la scansione a un pitch differente e quindi correggere il risultato.
5.3.2 Condizioni operative
La dose dipende da tutti quei parametri che agiscono sulla fluenza di fotoni in uscita che è generalmente proporzionale a: tensione, corrente nel tubo, tempo di scansione e spessore dello strato. In fantocci di PMMA, ad esempio, la dose aumenta approssimativamente del 40% passando da 120 kV a 140 kV a parità di corrente anodica.
Talvolta vengono utilizzati filtri diversi per la modulazione del fascio, come per le scansioni della testa e del corpo; talvolta possono essere anche introdotti dei filtri piatti per alcuni tipi particolari di esami come quelli pediatrici o per fluoroscopia e ciò modifica i valori della dose. La misura all’isocentro del CTDI100 in aria può non mostrare tali differenze essendo lo spessore della sezione al centro invariata. Qualora si volesse caratterizzare l’effetto sulla dose della forma del filtro è possibile effettuare un’ulteriore misura della dose in aria libera eseguita fuori asse, con la camera spostata lateralmente di 10 cm. La misura di dose in questo punto è dovuta al fascio RX che attraversa diversi spessori del filtro e quindi risente dell’effetto integrale del filtro sagomatore. Alcuni tomografi recenti hanno distanze fuoco asse di rotazione variabili, implementati con differenti campi di vista, e questo influenza la dose. Anche la dimensione del fuoco può influenzare leggermente la dose in modo particolare per spessori sottili.
Mentre il numero di fotoni aumenta all’aumentare dello spessore irradiato, la dose media, data dal CTDI, è generalmente costante poiché lo spessore nominale è incorporato nella definizione del CTDI. Quando si effettuano misure di CTDI in tomografi a singolo strato, i valori di CTDI100 sono costanti con lo spessore dello strato per gli strati più ampi. Tuttavia, per spessori più sottili, come per 2 o 1 mm, i valori risultano più alti in alcuni tomografi, in quanto lo spessore effettivamente irradiato è maggiore dello spessore della strato nell’immagine (post collimazione).
In un tomografo multistrato l’ampiezza del fascio utilizzato è maggiore di quella che è richiesta in un tomografo a singolo strato in modo da assicurare che tutti i rivelatori siano uniformemente irraggiati (overbeam). Questa è generalmente una quantità fissata e di conseguenza la porzione che riceve un irraggiamento “extra” diventa più grande per collimazioni più strette. Il CTDI100 aumenta quindi gradualmente al diminuire della collimazione. Tale aumento diventa significativo per collimazioni inferiori ai 10 mm.
Sia per i tomografi multistrato che per quelli a singolo strato, il rapporto tra CTDI100 per differenti spessori dello strato tende ad essere simile se misurato in aria o in fantoccio nonostante in fantoccio ci sia una maggior quantità di radiazione diffusa. Tali rapporti possono essere meno sovrapponibili nella MSTC all’aumentare dello spessore irradiato per l’aumento della radiazione diffusa al di fuori della camera a ionizzazione.
5.3.3 Commenti
Il documento IPEM 91 [34] raccomanda la misura del CTDI in aria per le prove di costanza.
Il documento Europeo “European Guidelines on Quality Criteria for Computed Tomography“ [24] utilizza invece il CTDIw, cioè un indice pesato di dose assorbita in aria a partire da misure in fantoccio di PMMA, in quanto più vicino alla dose assorbita dal paziente. Tale valore non include la correzione per il pitch. Poiché il CTDIw viene utilizzato per il calcolo del DLP, allora l’influenza del pitch sarà inclusa in tale valutazione.
Anche il documento IEC [30] utilizza come standard dosimetrico il CTDIw. Inoltre lo standard di sicurezza richiede che il CTDIw sia indicato sulla consolle del tomografo. Nella ultima edizione delle Norme IEC [41], tuttavia, la norma prevede che il CTDIw sia corretto per il pitch e che sia questo valore ad essere indicato sulla consolle (CTDIvol).
Indicare il CTDIw corretto per il pitch risulta tuttavia in conflitto con la definizione riportata nel documento della Commissione Europea .
Pertanto il calcolo del DLP, a partire dal valore di CTDIw visualizzato alla consolle utilizzando la definizione della CE, risulterebbe errato poiché il pitch verrebbe conteggiato due volte.
E’ quindi fondamentale che l’esperto in fisica medica, come già detto, effettui dei test di controllo che verifichino non solo la correttezza del valore che compare sulla consolle, ma anche se questo sia o meno corretto per il pitch.
5.3.4 Strumentazione utilizzata
Per le misure di dose si utilizzano una camera a ionizzazione a stilo (10 cm), un elettrometro e i fantocci dedicati in PMMA con diametri da 32 cm e 16 cm. Nel caso di utilizzo di dosimetri a termoluminescenza, i TLD100 al fluoruro di Litio, opportunamente calibrati, sono tra i più indicati.
La dose di radiazione è direttamente dipendente dalle dimensioni e dalla composizione del fantoccio.
5.4 Prodotto dose lunghezza (DLP)
Il DLP fornisce informazioni sull’esposizione totale nel caso di un esame TC completo; rappresenta il prodotto della dose media moltiplicata per la lunghezza della scansione. Può essere calcolato in diversi modi, utilizzando il CTDIw e i parametri di scansione come il numero di strati, la lunghezza della scansione e il pitch, o il tempo totale della scansione. Tuttavia, la relazione, fornita dalle Linee Guida Europee sui criteri di qualità dell’immagine e dosi di riferimento in TC, rappresenta il metodo standard. L’utilizzo del tempo totale di irraggiamento permette di non utilizzare il pitch in modalità spirale.
Le definizioni della CE sono state concepite per tomografi a singolo strato, tuttavia esse possono essere adattate anche a tomografi multistrato come scritto sotto. Per le scansioni sequenziali la definizione può esser applicata direttamente:
(5.8) DLP = nCTDIw × C × N × T scansione sequenziale
Dove:
nCTDIw = CTDI normalizzato e pesato (mGy/mAs)
C = esposizione radiografica per singolo strato (mAs)
N = numero totale di strati acquisiti
T = spessore nominale dello strato o del gruppo di rivelatori in un
tomografo multistrato
La definizione spirale può essere applicata anche ai tomografi multistrato estendendo la definizione del T all’ampiezza totale dei rivelatori attivi durante l’acquisizione (n × T):
(5.9) DLP = nCTDIw × A × t × n × T scansione spirale
Dove :
nCTDIw = CTDI normalizzato e pesato (mGy/mAs)
A = corrente del tubo (mA)
t = tempo si scansione del volume
n = numero di strati acquisiti simultaneamente
T = spessore nominale dello strato o del gruppo di rivelatori in un
tomografo multistrato
Il prodotto (n × T) è l’ampiezza totale dei rivelatori utilizzati con un tomografo multistrato ed è equivalente all’ampiezza nominale del fascio.
5.5 Nuove definizioni – ICRU 74
La pubblicazione n.74 dell’ICRU “Patient Dosimetry for X Rays used in Medical Imaging” del 2005 [50] definisce in modo sistematico e armonizzato tutte le grandezze dosimetriche utili e collegate alla dosimetria del paziente per tutte le applicazioni dei raggi X nell’imaging medico. Nel caso della TC questa revisione riguarda la definizione di CTDI e DLP sia in aria che in fantoccio.
La pubblicazione richiama il lettore alla differenza tra kerma in aria e dose assorbita, partendo dalle seguenti considerazioni: la produzione di Bremsstrahlung per le energie di fotoni utilizzate nell’imaging medico è trascurabile in mezzi a basso numero Z (10-3 o 10 -4), come i tessuti corporei . L’equilibrio elettronico è raggiunto immediatamente nei tessuti a basso Z perché il range degli elettroni secondari è molto inferiore al libero cammino medio dei fotoni RX.
Quando sono verificate queste due condizioni, il kerma in aria e la dose in aria risultano numericamente uguali. Nell’imaging medico questa condizione è verificata sempre, a meno delle interfacce tra mezzi a densità molto diversa.
In definitiva, poiché la grandezza che si misura nell’imaging medico è il kerma in aria ed è a questa grandezza che si riferiscono le condizioni di taratura, per evitare ambiguità è giusto riferirsi sempre a questa grandezza.
Nel caso in cui non sia stabilito l’equilibrio elettronico, la differenza tra le due grandezze può essere più importante (20%-35%) e risulta più appropriato utilizzare il kerma in aria piuttosto che la dose assorbita in aria.
Nel caso della TC, questo significa modificare le definizioni di Computed Tomography Dose Index in Computed Tomography air-Kerma Index:
(5.10)
dove K(z) è il profilo del kerma in aria lungo l’asse z.
Questa definizione è valida sia per le misure in aria libera, sia per le misure in fantoccio. Nel secondo caso, K(z) sarà il kerma in aria misurato dentro la cavità del fantoccio.
A partire dalla definizione 5.10 risulta necessario modificare di conseguenza anche le grandezze derivate come il CTDIw, il CTDIvol e il DLP.
Nonostante questa importante revisione delle definizioni e della simbologia, occorre rilevare che la pubblicazione ICRU 74 non modifica le modalità operative di misura, che pertanto rimangono invariate e non si pongono problemi pratici di ridefinire le misure di dose già implementate o sostituire la strumentazione in uso.
6 DOSIMETRIA DEL PAZIENTE
Le misure dosimetriche effettuate nei test di accettazione e di costanza possono essere utilizzate per confronti dosimetrici o per calcoli della dose efficace.
6.1 Confronti dosimetrici
Il CTDI100 è generalmente utilizzato per effettuare confronti tra tomografi e protocolli differenti. Viene misurato utilizzando i fantocci standard e pertanto in tale misurazione viene inclusa la radiazione diffusa, e l’energia efficace del fascio è più vicina a quella trovata nel paziente rispetto alle misurazioni effettuate in aria. Il CTDIw combina le misure di dose (CTDI100) al centro e alla periferia del fantoccio in un unico valore.
Per confrontare tomografi di differenti modelli, il CTDIw è misurato in ciascun tomografo usando spessori dello strato, kV e mAs tipici. Il nCTDIw normalizzato (mGy/mAs) non dovrebbe essere utilizzato per confrontare tomografi differenti perché spesso la differenza del valore di nCTDIw è giustificata da differenze nelle distanze fuoco-isocentro, fuoco rivelatore e filtrazione del fascio.
6.1.2 Confronto tra protocolli
Il confronto tra generici protocolli senza la variabile della lunghezza acquisita può essere effettuato valutando la dose relativa.
Il CTDIw è misurato utilizzando valori di spessore dello strato, kV e mAs tipici di un determinato protocollo. Il CTDI è generalmente lineare con i mAs e, per tomografi a singolo strato è costante con lo spessore dello strato eccetto che per strati sottili. Per tomografi multistrato il CTDIw cresce al diminuire dello spessore dello strato. Per completezza devono essere misurati anche gli effetti della filtrazione e dei kV.
L’effetto dell’incremento del lettino e del pitch può essere incluso mediando il CTDIw lungo l’asse z in modo tale da ottenere il CTDI mediato lungo l’asse z o corretto per il pitch (CTDIvol).
6.1.3 Confronto tra rischi
Utilizzando la lunghezza totale acquisita, si può calcolare il DLP come prodotto dose (CTDIw) × lunghezza, che può essere impiegato per confrontare il rischio da radiazione per il paziente per esami specifici .
E’ importante utilizzare il CTDIw senza alcuna correzione per il pitch, poiché la definizione di DLP data nella Sezione 5.4 utilizza il tempo totale di irraggiamento che tiene già conto del pitch utilizzato nell’acquisizione spirale.
6.2 Dose superficiale e agli organi
La dose superficiale e agli organi può essere misurata utilizzando una serie di TLD al fine di ottenere la MSAD come descritto nella sezione 5.3. La dose superficiale nel caso di un paziente o di un fantoccio può essere misurata in questo modo con TLD incapsulati in un idoneo contenitore. Per coprire le variazioni del profilo della MSAD e per fornire un valore medio corretto deve essere posizionato lungo l’asse z un numero sufficiente di TLD.
In alternativa può essere utilizzata anche una camera a ionizzazione in modo tale che venga irradiata l’intera lunghezza della camera.
La stima della dose agli organi interni può essere ottenuta utilizzando un fantoccio adatto come per esempio il fantoccio Alderson Rando.
6.3 Dose Efficace
Quando è richiesto il calcolo della dose efficace, possono essere utilizzati i dati riportati dall’NRPB, insieme ai valori di CTDI100 misurati in aria.
Questi dati sono stati ottenuti utilizzando calcoli Monte Carlo sull’interazione dei raggi X in un fantoccio matematico ermafrodito, utilizzando informazioni sullo spettro del fascio e la filtrazione fornite dal costruttore; sono utilizzati per calcolare la dose agli organi e la dose efficace per tomografi specifici e parametri specifici. Inoltre, poiché i dati sono ottenuti a partire da un fantoccio ermafrodito di una fissata dimensione, questi possono essere utilizzati solo per una valutazione approssimativa della dose agli organi e dalla dose efficace per ciascun paziente.
Tali dati possono essere modificati utilizzando programmi software anche “realizzati in casa”, o ottenuti commercialmente come elencato nella tabella 6.1. I dati di dose agli organi sono normalizzati alla dose in aria valutata all’isocentro. Una misura di CTDI in aria per un dato tomografo pertanto è fondamentale per il calcolo della dose agli organi .
CT-Dose Baadegaard N, Jensen LC (1999) A CT dose calculation software “CT-Dose”. National Board of Health, Aarhus University Hospital, Denmark.
NRPB Jones DG, Shrimpton PC (1993) Normalized organ doses for X-Ray computed Tomography calculated using Monte Carlo techniques NRPB-SR250.
Windose Kalender WA, Schmidt B, Zankl M, Schmidt M (1999) A PC program for estimating organ dose and effective dose values in computed tomography. Eur Radiol 9:555-562.
CT-EXPO Brix G et al. Assessment of a theoretical formalism for dose estimation in CT: an anthropomorphic phantom study. Eur Radiol.14(7):1275-84.
CTDosimetry N. Keat, ImPACT, UK, http://www.impactscan.org/ctdosimetry.htm .
eXpoDOSE N.A. Gkanatsios and W Huda , http://www.exodose.com (Nuclear Associates)
P-Dose/
CT Module Evaluation of Organ Doses for CT examination, CyberQual SRL Gorizia, Italy
Tabella 6.1 Alcuni software basati su simulazioni Montecarlo per il calcolo della dose efficace e agli organi.
7. Il parametro Q
Il rumore, la risoluzione spaziale e lo spessore dello strato sono parametri che descrivono la “quantità” di informazioni che si possono ottenere da un’immagine. La dose può essere considerata come il “costo” che si deve pagare per ottenere tali informazioni; non ha significato riferirsi ad una sola di queste grandezze senza collegarsi anche alle altre [3, 23, 26, 27]
Il parametro Q, introdotto da Impact (MDA – Department of Health – UK), è un indice sintetico della qualità dell’immagine e della dose che riassume in un solo numero informazioni riguardanti il rumore, la risoluzione spaziale, lo spessore dello strato e la dose. E’ definito come:
(7.1)
dove:
σ è il rumore dell’immagine; fav è un indice della risoluzione spaziale ed è dato da (MTF50%+MTF10%)/2, dove MTF50% e MTF10% sono le frequenze spaziali corrispondenti al 50% e al 10% della curva MTF, espressi in coppie di linee per cm; z è lo spessore dello strato.
Il valore Q è inversamente proporzionale alla dose, allo spessore dello strato e al rumore mentre è direttamente proporzionale alla risoluzione spaziale. Un’acquisizione che presenti un buon bilancio di questi parametri sarà caratterizzata da un valore alto di Q che quindi esprime un buon compromesso dose-qualità immagine.
La 7.1 deriva dalla seguente relazione di proporzionalità:
(7.2)
Il rumore è infatti legato al numero di fotoni N da una proporzionalità inversa:
(7.3)
e il numero di fotoni N è a sua volta proporzionale allo spessore dello strato e ai mAs (quindi alla dose):
(7.4)
La (7.1) presuppone che tra rumore e risoluzione spaziale esista una relazione del tipo [28]
(7.5)
In realtà la (7.5) non è valida per i tomografi e i filtri di convoluzione correntemente utilizzati, e deve essere determinata sperimentalmente per ogni tomografo, misurando il rumore dell’immagine e la risoluzione spaziale per diversi filtri di convoluzione, mantenendo costante la dose e lo spessore dello strato
I valori sperimentali a disposizione mostrano che l’andamento è di tipo esponenziale e che l’esponente è generalmente compreso tra 4 e 5 ed è differente tra filtri Body e Head.
Il significato e l’utilizzo di questo parametro non è immediato. La sua utilità nel processo di ottimizzazione dei protocolli clinici non è semplice in quanto il parametro tende ad elidere le dipendenze dagli indicatori di qualità (rumore, risoluzione spaziale) rispetto alla dose fino ad arrivare ad un indice di “qualità intrinseca” più utile forse per i confronti tra apparecchiature.
8. VERIFICHE DI ACCURATEZZA MECCANICA
8.1. Introduzione
I controlli di accuratezza meccanica permettono di verificare il corretto posizionamento del paziente sottoposto a un’indagine tomografica.
I dispositivi che devono essere controllati sono: le luci di posizionamento del paziente, il movimento lettino portapaziente e il gantry.
Le modalità di misura, l’accuratezza e i limiti di accettabilità dipendono dalle finalità di impiego del tomografo computerizzato; per i tomografi computerizzati utilizzati per produrre immagini utilizzate per il calcolo dei piani di trattamento l’accuratezza dei dispositivi di posizionamento è più critica.
8.2 Tomografi computerizzati per impiego diagnostico
Si riportano le verifiche di accuratezza meccanica suggerite dal documento “ImPACT CT Scanner Acceptance test” [29] da eseguire in fase di accettazione di una apparecchiatura per tomografica computerizzata.
Coincidenza della luce interna del gantry e luce di posizionamento esterna del gantry
Coincidenza della luce interna del gantry con il piano di scansione
Accuratezza delle luci nel piano sagittale e coronale per la determinazione dell’isocentro del gantry
Accuratezza degli indicatori di posizione del gantry
Accuratezza dell’intervallo di acquisizione in modalità assiale
Accuratezza dello spostamento del lettino in modalità spirale
Accuratezza dell’angolo di inclinazione del gantry
Tutti i controlli sono di facile e rapida esecuzione. I dispositivi di prova necessari sono: un righello, un ago o la punta di una penna, dei reperi metallici e una pellicola a bassa sensibilità.
Per le prove di costanza sui dispositivi di posizionamento del paziente si suggerisce di adottare le indicazioni fornite dalla norma CEI 62-59 [30], mentre per le prove di accettazione la norma CEI 62-135 [38].
8.3 Tomografi computerizzati per impiego in ambito radioterapico
I tomografi computerizzati utilizzati per produrre immagini utilizzate per il calcolo dei piani di trattamento radioterapico sono generalmente dotati di laser esterni, fissi o mobili, utilizzati per la marcatura del paziente. In questo caso è necessario verificare in fase di accettazione e periodicamente anche l’allineamento dei laser esterni e la distanza tra i laser esterni e i laser del gantry.
I dispositivi di misura utilizzabili per queste prove sono i medesimi fantocci impiegati per le verifiche di allineamento dei laser dei sistemi di simulazione e delle apparecchiature per teleradioterapia.
La periodicità dei controlli e le tolleranze dei parametri di misura dovrebbero essere uguali a quelli utilizzati sulle apparecchiature per terapia.
Il documento “Quality assurance for Computed-Tomography simulators and the computed tomography simulation process: Report of the AAPM Radiation Theraphy Committee Task Group n° 66“ [31] fornisce indicazioni metodologiche, periodicità e tolleranza applicabile ai tomografi computerizzati impiegati per uso radioterapico.
9 RICOSTRUZIONI MULTIPLANARI E 3-DIMENSIONALI
I tomografi non sono solo utilizzati per ricostruire strati transassiali. Il set di dati acquisiti può essere utilizzato per ricostruire l’immagine in altri piani così come per ricostruire immagini di volume. Gli standard di rappresentazione dei dati acquisiti sono ad esempio le MPR (ricostruzioni multiplanare), o le ricostruzioni 3-dimensionali di superficie o di volume rendering; le ricostruzioni effettuate possono poi essere rappresentate in termini di MIP (proiezioni di massima intensità) oppure MinP (proiezioni di minima intensità). Nella letteratura c’è scarsa informazione circa le procedure di verifica di queste immagini; qui di seguito si fa qualche commento sulla ricostruzione MPR. Un aspetto importante della valutazione di immagini non transassiali che dovrebbe essere considerato è l’accuratezza delle dimensioni (scala) in particolare per le applicazioni radioterapiche o chirurgiche.
Per la risoluzione spaziale di una MPR si faccia riferimento a quanto detto nel capitolo relativo alla risoluzione spaziale (par.3.2).
Per valutare l’accuratezza della scala è sufficiente avere un oggetto di dimensioni note lungo ciascuno dei piani ricostruiti. In alternativa si può utilizzare un oggetto con dei reperi parzialmente radiopachi che permetta di valutare le distanze almeno lungo i 3 piani. Si possono acquisire scansioni assiali anche se è preferibile effettuare acquisizioni spirali poiché sono le più utilizzate nella pratica clinica per la ricostruzione clinica multiplanare o 3-dimensionale. Le immagini assiali ricostruite a partire dall’acquisizione spirale è bene che abbiano un passo di ricostruzione inferiore a 1 per rotazione (strati sovrapporsti) per verificare la corretta riformattazione delle immagini (si sono riscontrati errori quando strati sovrapposti vengono trattati dall’elaborazione MPR come strati non sovrapposti dando luogo a ricostruzioni coronali allungate).
Si utilizza quindi il software di misura del tomografo per verificare le dimensioni riprodotte su ciascun piano ricostruito.
Il controllo di qualità del software eseguito dal costruttore dovrebbe essere adeguato, tuttavia sembra opportuno rivalutare queste misure dopo ogni aggiornamento o dopo l’installazione di nuovi pacchetti di ricostruzione. I pacchetti potrebbero essere installati separatamente o solo per il tomografo e per la stazione di lavoro. Se installati su entrambi è possibile che vengano installate due diverse versioni, cosa che va tenuta in considerazione. Come già discusso, il livello del controllo deve riflettere la significatività e l’accuratezza richieste dall’applicazione in esame.
Appendice I – Riferimenti relativi ai fantocci, camere a ionizzazione e software
Fantocci per QA
Catphan Phantom(CTP): The Phantom Laboratory, USA
RMI Phantom: Gammex-RMI (Radiation Measurement Incorporated) Ltd
AAPM Phantom: Nuclear Associates, CIRS o Capintec
CIRS Computed Tomography Imaging Reference Systems
QRM : Quality Assurance for Radiology and Medicine
Fantocci per Densità elettronica
RMI Electron Density Phantom: Gammex-RMI (Radiation Measurements Incorporated) Ltd
QRM : Bone Equivalent Synthetic Material for calibration
CIRS Electron Density Phantom Model 62
Camere a ionizzazione tipo “pencil”
Radcal Corporation (MDH)
Capintec Inc.
Vertec Scientific Ltd
PTW Freiburg
Scanditronix Wellhofer Dosimetry
RTI Electronics AB
Fantocci per la misura del CTDI in PMMA (perspex)
Capintec Inc.
Scanditronix Wellhofer Dosimetry (fantocci di materiale tessuto equivalente)
QRM
Dati e software sulla dose
Normalised Oragn Doses for X-ray Computed Tomography Calculated using Monte Carlo Techniques. NRPB-SR250. National Radiation Protection Board, UK
CTDOSE: John Leheron, National Radiation Laboratory, Christchurch, New Zeland
P-Dose/CT Module. Evaluation of Organ Doses for CT Examinations. CyberQual S.R.L. Gorizia, Italia
CTDosimetry.xls: N Keat, ImPACT, UK, http://www.impactscan.org7ctdosimetry.htm
WinDose: Scanditronix Wellhofer, http://www.wellhofer.com
CT-Expo v 1.0: G. Stamm and H.D. Nagel, http://www.tuev-nord.de/downloads/Leaflet_CT-expo.pdf
CT-Dose calculation program: N. Baadegaard & L.C. Jensen, http://www.mta.au.dk/ctdose
EXoDOSE: N.A. Gkanatsios and W. Huda, http://www.exodose.com
Indirizzi dei costruttori e dei fornitori
Capintec Inc., 6 Arrow Road, Ramsey, New Jersey, USA 07456
CIRS Computed Tomography Imaging Reference Systems, Inc., 2428 Almeda Avenue, Suite 212, Norfolk, Virginia 23513, USA. Internet: http://www.cirsinc.com
CyberQual S.R.L. Gorizia, Italia
Gammex-RMI (Radiation Measurements Incorporated) Ltd, Karlsruhe House, Queens Bridge Road, Nottingham NG2 1NB http://www.gammex.com
ISP International Specialty Products 1361 Alps Road, Wayne, NJ 07470 http://www.ispcorp.com
National Radiation Protection Board, Chilton, Didcot, Oxon OX11 0RQ
National Radiation Laboratory, PO Box 25099, Christchurch, New Zealand
Nuclear Associates, 120 Andrews Road , Hickville, NY 11801
Quados, Unit 8, Lakeside Business Park, Swan Lane, Sandhurst GU47 9DU
PTW-Freiburg Lörracher Strasse 7, D-79115 Freiburg, Germany
QRM- Dorsfstr. No.4, D -91096 Mohrendorf, Germany; http://ww.qrm.de
Radcal Corporation (MDH), 426 West Duarte Road, Monrovia, CA 91016-4591
Scanditronix Wellhofer dosimetry, http://www.scxmedical.se, http://www.wellhofer.com
The Phantom Laboratory, Post Office Box 511, Salem, New York, 12865-0511 http://www.phantomlab.com
Vertec Scientific Ltd, 5 Comet House, Calleva Park, Aldermaston, reading RG7 8JA
RTI Electronics AB Goteborgsvagen 97/50 SE-431 37 Molndal Sweden
Schema dei principali fantocci per QA
Fig I.1: schema GAMMEX 464 (fantoccio utilizzato per l’accreditamento ACRT in USA) [42]
Fig I.2: SCHEMA CATPHAN 500 E 600 [35]
Fantocci che soddisfano le linee guida AAPM Report n.1 e “Performance Evaluation and QC of CT Scanners”, Report n.39 “Specification and Acceptance Testing of Computed Tomography Scanners”
Fig I.3: CIRSINC Modello 610 [36]
Fig I.4: CAPINTEC (0695-0105) [45]
Fig I.5: Nuclear Associates 76-410-4130 [44]
Appendice II TC-PETIntroduzione
La TC è una modalità di imaging tridimensionale che fornisce immagini anatomiche con risoluzione sub-millimetrica. La PET (tomografia a emissione di positroni) produce immagini 3D che riflettono informazioni fisiologiche in quanto mostrano la captazione di radiofarmaci emittenti positroni iniettati nel paziente. I tomografi TC/PET combinano queste due modalità di imaging, consentendo di ottenere in un’unica sessione sia immagini anatomiche che immagini funzionali.
Tomografi TC/PET
I sistemi TC/PET attualmente disponibili sul mercato sono costituiti da in un unico gantry con i sistemi PET e TC adiacenti l’uno all’altro. In alcuni sistemi viene utilizzata un’unica “cuffia” per i due gantry, in altri i gantry hanno “cuffie” separate posizionate una vicino all’altra.
I sistemi TC sono generalmente quelli già disponibili sul mercato come sistemi separati, con le stesse caratteristiche di qualità dell’immagine e di dose.
Il paziente solitamente viene sottoposto a una scansione TC nella prima parte dell’esame (figura II.1a), successivamente il lettino viene fatto avanzare nel gantry per eseguire la scansione PET (figura II.1b).
Figura II.1: sistema TC/PET [32]
Registrazione di immagini TC/PET
Le immagini PET contengono pochi dettagli anatomici e vengono spesso analizzate insieme ad immagini TC per aiutarsi nella localizzazione di aree di captazione del tracciante. Nel passato, le immagini PET e TC venivano acquisite separatamente, e il paziente doveva spostarsi da un tomografo all’altro. Erano disponibili stazioni di lavoro per registrare le immagini PET e TC utilizzando reperi anatomici per tenere conto del diverso posizionamento del paziente nelle due scansioni; tali reperi dovevano essere costituiti di un materiale visibile sulle immagini in entrambe le modalità. Questa tecnica era appropriata soprattutto per regioni corporee immobili, come ad esempio l’encefalo. Gli organi in altre regioni anatomiche (es: addome) sono mobili, e cambiano quindi posizione nelle due acquisizioni. Questo rendeva il processo di registrazione di immagini più difficoltoso e quindi meno accurato.
Con l’avvento di sistemi TC/PET il problema della registrazione delle immagini si è semplificato: gli esami PET e TC vengono acquisiti in sequenza, senza che il paziente si sposti da un tomografo all’altro. Questo elimina i problemi di registrazione delle immagini sopra citati. Una volta terminato l’esame TC, il lettino del paziente viene spostato nel gantry delle PET per eseguire il secondo esame. I due set di dati si possono considerare già registrati; bisogna solo tenere in considerazione la distanza tra le posizioni PET e TC.
Un altro problema legato alla registrazione è la flessione del lettino. Nella figura II.2 è rappresentato un lettino normalmente utilizzato in TC. Man mano che il lettino avanza nel gantry, aumenta la frazione di peso del paziente sostenuta della parte del lettino che non è supportata dalla base; si ha così una flessione del lettino man mano che lo stesso avanza nel gantry. Per una registrazione accurata è importante che il grado di flessione del lettino non cambi quando il paziente si sposta dalle posizioni di acquisizione TC e PET; questo provocherebbe problemi nella registrazione delle immagini, perché quando il paziente si sposta dalla TC alla PET aumenta la flessione del lettino e quindi la posizione del paziente durante l’esame PET è più bassa di quella durante l’esame TC. Questa differenza nella posizione verticale dipende dal peso del paziente.
Figura II.2: lettino per TC [32]
Per ridurre questo problema di flessione sono stati creati lettini speciali (figura II.3): il lettino è fissato a un piedistallo mobile e il sistema lettino-piedistallo si muove dentro e fuori il gantry.
Quando il paziente è sdraiato sul lettino, questo avrà un certo grado di flessione, ma il grado di flessione rimane costante indipendentemente da quanto il lettino viene spostato nel gantry. Questo assicura che la posizione verticale del paziente sia la stessa per le acquisizioni TC e PET.
Figura II.3: lettino per TC/PET [32]
Accuratezza di registrazione
E’ necessario verificare l’accuratezza della registrazione di immagini TC e PET; a questo scopo si utilizza un fantoccio contenente una distribuzione tridimensionale nota di oggetti, visibile sia in TC che in PET. Utilizzando il software di fusione in dotazione al sistema, si può eseguire la registrazione delle immagini e verificare l’accuratezza.
Correzione per l’attenuazione
L’assorbimento e lo scattering dei fotoni a 511 keV porta a una diminuzione del tasso di conteggio dei rivelatori: alcune aree dell’immagine PET mostrano livelli di attività che sono inferiori al loro valore vero. Per correggere questo fenomeno si possono utilizzare delle mappe di attenuazione del paziente. I sistemi PET tradizionali effettuano questa correzione utilizzando delle sorgenti radioattive lineari che misurano l’attenuazione nel paziente. L’acquisizione di questi dati richiede parecchi minuti e fa aumentare considerevolmente la durata dell’intero esame. La deviazione standard dei valori di questa mappa di attenuazione è elevata, e questo influisce sicuramente sull’accuratezza delle immagini PET corrette.
In un sistema TC/PET, le immagini TC sono utilizzate per generare le mappe di correzione per l’attenuazione da applicare alle immagini PET. I valori dei pixel dell’immagine TC (espressi in unità Hounsfiled, HU) sono proporzionali al coefficiente di attenuazione del tessuto:
Queste mappe, confrontate con quelle ottenuto con sorgenti radioattive, sono più rapide da ottenere e hanno un rumore più basso; inoltre consentono di ridurre la durata dell’esame del 30-40% e, conseguentemente, la probabilità di movimento del paziente.
Dipendenza dall’energia delle mappe di attenuazione
I dati TC sono raccolti utilizzando raggi X con un picco energetico di 120 keV e un’energia media di circa 70 keV. I coefficienti di attenuazione dipendono dall’energia, quindi le mappe di attenuazione ricavate dalla TC devono essere adattate prima di essere applicate elle immagini PET (511 keV). A tale scopo, uno dei metodi più utilizzati consiste nel fornire una conversione tra i numeri TC e il coefficiente di attenuazione PET utilizzando una scala bilineare (figura II.4)
Figura II.4: coefficienti di attenuazione PET in funzione dei numeri TC [32]
Dose
Nella maggior parte degli esami TC/PET la scansione TC può non essere di qualità diagnostica, perché le immagini TC devono essere usate solo per generare le mappe di correzione per l’attenuazione. Di conseguenza, le immagini TC possono avere qualità “bassa”, essere acquisite con fattori di esposizione bassi in modo da ridurre nella maggior misura possibile la dose al paziente. Solitamente nei sistemi TC/PET i tomografi TC lavorano con una corrente nel tubo più bassa (circa la metà di quella usata in diagnostica), 70-80 mA. Questo può però causare artefatti.
La dose al paziente in seguito ad esami TC dipende dal protocollo utilizzato e dalla regione anatomica esaminata. Con i parametri di acquisizione comunemente utilizzati in diagnostica, si hanno dosi efficaci di 1-3 mSv per esami del cranio; di 5-20 mSv per scansioni della regione addominale dipendentemente dall’estensione della regione analizzata. Se il tomografo viene fatto lavorare a una tensione più bassa, con correnti più basse (70-80 mA), le dosi si dimezzano. In ogni modo per esami total body, la scansione TC contribuisce significativamente alla dose al paziente.
La dose al paziente per la componente PET dell’esame è di circa 10 mSv.
Appendice III PROTOCOLLO PROVE DI ACCETTAZIONE
Introduzione
Viene proposta in questa Appendice una traccia da seguire nella stesura di un protocollo di misure per una prova di accettazione di un Tomografo Computerizzata Multistrato: per le modalità operative si rimanda ovviamente alla descrizione dettagliata del testo. Questo schema tiene conto delle indicazioni della Norma CEI 62-135 [38] oltre che delle indicazioni fornite da altri organismi scientifici internazionali [34] .
Esame a vista e prove di funzionamento
Alta Tensione e Filtrazione totale (opzionali)
Questi test possono essere eseguiti in collaborazione con i tecnici della ditta costruttrice.
Qualità dell’immagine
Rumore
In acquisizione sia assiale che spirale e al variare del pitch
Uniformità dei numeri TC
Acquisizione assiale
N. TC e linearità
Acquisizione assiale (se le immagini TC verranno usate anche per la pianificazione di trattamenti effettuare la misura anche in acquisizione spirale con i protocolli specifici)
Risoluzione spaziale
Acquisizione assiale
Risoluzione a basso contrasto
Risoluzione spaziale lungo Z
Artefatti
Acquisizione spirale
Caratteristiche dello strato
Spessore dello strato
Acquisizione assiale
Acquisizione spirale (SSP)
Spessore irradiato
Acquisizione assiale
Efficienza geometrica
Indici di dose
CTDI in aria
(se possibile valutare per tutte le configurazioni)
CTDIw in fantoccio
CTDIvol in spirale
Accuratezza meccanica e controlli geometrici
Per l’esecuzione di questi controlli dal punto di vista pratico si rimanda alla norma CEI 62-135 e al documento www.impactscan.org/download/acceptancetestingdownload.htm mentre per i valori di riferimento alle specifiche delle Ditte costruttrici
BIBLIOGRAFIA